Hvad er de kemiske egenskaber, når kaliumcarbonat tilsættes til HCL?
Produkter:
* kuldioxid (co₂): Denne gas produceres som bobler og er ansvarlig for den fizzing, der er observeret i reaktionen.
* kaliumchlorid (KCL): Dette er et opløseligt salt, der forbliver opløst i opløsningen.
* vand (H₂O): Dette dannes også som et produkt af reaktionen.
Kemisk ligning:
K₂co₃ (aq) + 2 HCI (aq) → 2 kCl (aq) + h₂o (l) + co₂ (g)
Forklaring:
* Reaktionen er en dobbeltfortrængningsreaktion hvor de positive og negative ioner af reaktanterne skifter steder.
* Karbonationen (co₃²⁻) reagerer med hydrogenionerne (H⁺) fra HCI til dannelse af kulsyre (H₂co₃).
* Kulsyre er ustabil og nedbrydes hurtigt i kuldioxid (CO₂) og vand (H₂O).
* Kaliumionerne (K⁺) og chloridioner (CL⁻) forbliver opløst i opløsningen som kaliumchlorid (KCL).
Kemiske egenskaber:
* eksotermisk reaktion: Reaktionen frigiver varme, hvilket gør opløsningen varm.
* Gasudvikling: Dannelsen af kuldioxidgas er en karakteristisk observation af denne reaktion.
* neutralisering: Reaktionen neutraliserer HCls sure egenskaber.
* saltdannelse: Kaliumchlorid, et salt, produceres som et produkt.
Sikkerhedsforholdsregler:
* Tilsæt altid kaliumcarbonat til syreopløsningen langsomt og forsigtigt for at undgå kraftig boblende og potentiel sprøjtning.
* Udfør reaktionen i et godt ventileret område eller brug en røghætte til at undgå indånding af kuldioxidgas.
* Bær passende sikkerhedsudstyr, såsom beskyttelsesbriller og handsker.
Sidste artikelKemisk formel til kalium og klor?
Næste artikelHvor mange atomer i BR2?
 Varme artikler
Varme artikler
-
 Sådan bygger du effektive organiske solcellerFeng Gao, lektor ved Linköpings Universitet, Sverige. Kredit:Göran Billeson Organiske solceller, lavet af kulstofbaserede materialer, frembyder unikke fordele sammenlignet med andre solcelleteknol
Sådan bygger du effektive organiske solcellerFeng Gao, lektor ved Linköpings Universitet, Sverige. Kredit:Göran Billeson Organiske solceller, lavet af kulstofbaserede materialer, frembyder unikke fordele sammenlignet med andre solcelleteknol -
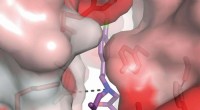 Målrettet skjult lomme til behandling af slagtilfælde og anfaldEn kemisk forbindelse i 93-serien slutter sig til en neurons NMDA-receptor. Forbindelser som denne har en høj affinitet for receptoren på grund af et unikt motiv, der trækkes ind i en skjult lomme (il
Målrettet skjult lomme til behandling af slagtilfælde og anfaldEn kemisk forbindelse i 93-serien slutter sig til en neurons NMDA-receptor. Forbindelser som denne har en høj affinitet for receptoren på grund af et unikt motiv, der trækkes ind i en skjult lomme (il -
 Forskere konstruerer verdens første aerogeler lavet af skrotdækEt hold af NUS-forskere ledet af professor Duong Hai-Minh (forreste række, først fra venstre) og prof Nhan Phan-Thien (forreste række, centrum), udviklet verdens første aerogel fremstillet af skrotgum
Forskere konstruerer verdens første aerogeler lavet af skrotdækEt hold af NUS-forskere ledet af professor Duong Hai-Minh (forreste række, først fra venstre) og prof Nhan Phan-Thien (forreste række, centrum), udviklet verdens første aerogel fremstillet af skrotgum -
 Forudsigelse af avanceret medicinsk udstyrs nedbrydningsadfærdKredit:Cell Reports Physical Science af Cell Press. Polymermaterialer spiller en afgørende rolle i nutidens medicin. Mens mange applikationer kræver langtidsholdbare enheder, andre nyder godt af m
Forudsigelse af avanceret medicinsk udstyrs nedbrydningsadfærdKredit:Cell Reports Physical Science af Cell Press. Polymermaterialer spiller en afgørende rolle i nutidens medicin. Mens mange applikationer kræver langtidsholdbare enheder, andre nyder godt af m
- Den nemme måde at få et firkantet tilbud på
- Samarbejdende videnskabsmænd giver indsigt i at forbedre blå OLED-ydeevne til skærme og belysning…
- At falde til jorden tager lang tid
- Hvor meget nitrogen er der for majs?
- Hvilken halogenbrom eller jod vil danne den mere polære binding med fosfor?
- Sammenlign og kontrast granitdiorit?


