Hvilket element ville ionisk bindes med klor?
Her er nogle eksempler på metaller, der ville binde ionisk med klor:
* natrium (NA): Natrium er i gruppe 1, hvilket betyder, at det har en valenselektron, som det let mister for at danne en +1 ion (Na +). Dette danner natriumchlorid (NaCl) , almindeligt kendt som bordsalt.
* kalium (k): I lighed med natrium er kalium også i gruppe 1 og danner en +1 ion (K +). Dette danner kaliumchlorid (KCL) , brugt i gødning og medicin.
* magnesium (mg): Magnesium er i gruppe 2 og mister let to elektroner til dannelse af en +2 ion (Mg2 +). Dette danner magnesiumchlorid (MGCL2) , brugt i afisningsmidler og som tørringsmiddel.
* calcium (CA): I lighed med magnesium er calcium i gruppe 2 og danner en +2 ion (Ca2 +). Dette danner calciumchlorid (CACL2) , brugt som tørringsmiddel og i vejsalt.
Generelt har metaller fra grupper 1 og 2, såvel som nogle overgangsmetaller, en tendens til at danne ioniske bindinger med klor.
Sidste artikelHvad er sammensætningen af WPS -metal?
Næste artikelHvad er formlen for Triphosphorus octachloride?
 Varme artikler
Varme artikler
-
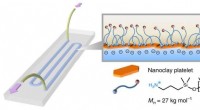 Bro over koblede farvande:Forskere 3-D-printer laboratorium med fuld væske på en chipNår to væsker - den ene indeholder nanoskala lerpartikler, en anden indeholdende polymerpartikler - er trykt på et glassubstrat, de kommer sammen ved grænsefladen mellem de to væsker og danner inden f
Bro over koblede farvande:Forskere 3-D-printer laboratorium med fuld væske på en chipNår to væsker - den ene indeholder nanoskala lerpartikler, en anden indeholdende polymerpartikler - er trykt på et glassubstrat, de kommer sammen ved grænsefladen mellem de to væsker og danner inden f -
 Kirurgi i en pille en potentiel behandling for diabetesOperation i en pille i tarmen. Kredit:Brigham and Womens Hospital og Randal Mckenzie I løbet af det sidste årti, bariatriske kirurger har gjort fremskridt med at udføre vægttabskirurgi, der ikke k
Kirurgi i en pille en potentiel behandling for diabetesOperation i en pille i tarmen. Kredit:Brigham and Womens Hospital og Randal Mckenzie I løbet af det sidste årti, bariatriske kirurger har gjort fremskridt med at udføre vægttabskirurgi, der ikke k -
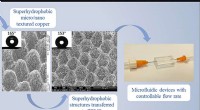 Ny fremstillingsproces skaber supersmå kanaler til at afvise vand og forbedre medicinsk, elektronis…Dette billede viser skabelsen af en superhydrofob overflade på en metaloverflade med en ultrahurtig laser, som overføres til PMDS via transferstøbning og samles til en mikrofluidisk enhed. Kredit:Pu
Ny fremstillingsproces skaber supersmå kanaler til at afvise vand og forbedre medicinsk, elektronis…Dette billede viser skabelsen af en superhydrofob overflade på en metaloverflade med en ultrahurtig laser, som overføres til PMDS via transferstøbning og samles til en mikrofluidisk enhed. Kredit:Pu -
 Websted for datadeling kan fremskynde reaktionen på nye ulovlige stofferNPS DataHub giver retsmedicinske kemikere mulighed for at dele data om nye lægemiddelanaloger, herunder deres kemiske strukturer og signaturer, som er nøglerne til at identificere dem i laboratoriet.
Websted for datadeling kan fremskynde reaktionen på nye ulovlige stofferNPS DataHub giver retsmedicinske kemikere mulighed for at dele data om nye lægemiddelanaloger, herunder deres kemiske strukturer og signaturer, som er nøglerne til at identificere dem i laboratoriet.


