Hvad er molaliteten af en opløsningsklor og vand 0,0362 m hvor meget i gram blev brugt til at fremstille denne opløsning?
Forståelse af molalitet
* molalitet (m) er en måde at udtrykke koncentrationen af en opløsning på. Det er defineret som antallet af mol opløst stof (i dette tilfælde klor) pr. Kg opløsningsmiddel (vand).
Nøgleinformation
* molalitet (m) =0,0362 m
* opløst: Klor (cl₂)
* opløsningsmiddel: Vand (H₂O)
Beregninger
1. Antag en masse opløsningsmiddel: For at gøre dette problem lettere, lad os antage, at vi har 1 kg (1000 g) vand.
2. Beregn mol chlor: Da molalitet er mol -opløst stof pr. Kg opløsningsmiddel, kan vi beregne molen af klor:
* mol klor =molalitet × Masse opløsningsmiddel (i kg)
* mol klor =0,0362 m × 1 kg =0,0362 mol
3. Konverter mol til gram af klor:
* Vi har brug for den molære masse af klor (CL₂), som er ca. 35,45 g/mol * 2 =70,90 g/mol
* gram klor =mol klor × molmasse klor
* gram klor =0,0362 mol × 70,90 g/mol ≈ 2,57 g
Svar
Du har brug for cirka 2,57 gram af klor til at fremstille en 0,0362 molal opløsning i 1 kg vand.
 Varme artikler
Varme artikler
-
 Ny hybridelektrolyt til højtydende Li-ion-batterierEt fotografi (venstre), henholdsvis et scanningselektronmikroskopbillede (i midten) og en skematisk illustration af sammensat elektrolytstruktur (til højre). Kredit:Grewal og Yabu. Li-ion-batterier
Ny hybridelektrolyt til højtydende Li-ion-batterierEt fotografi (venstre), henholdsvis et scanningselektronmikroskopbillede (i midten) og en skematisk illustration af sammensat elektrolytstruktur (til højre). Kredit:Grewal og Yabu. Li-ion-batterier -
 Ny jernbaseret katalysator øger omdannelsen af CO2 til højere alkoholerAfslører den fremmende rolle af S i syntese af højere alkoholer over jernkatalysatorer. Kredit:YAO Ruwei Højere alkoholer (C 2+ Åh), vigtige mellemprodukter til finkemikalier, produceres hovedsa
Ny jernbaseret katalysator øger omdannelsen af CO2 til højere alkoholerAfslører den fremmende rolle af S i syntese af højere alkoholer over jernkatalysatorer. Kredit:YAO Ruwei Højere alkoholer (C 2+ Åh), vigtige mellemprodukter til finkemikalier, produceres hovedsa -
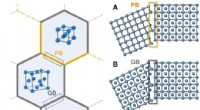 Brug af kemisk grænseteknik til at skabe stål, der er stærkt og fleksibelt uden højt kulstofindh…Skematisk illustration af en PB, en GB, og en CB. (A) PB, en grænse mellem to korn af forskellig gittertype. (B) GB, en grænse mellem to korn af samme gittertype, men med forskellige krystallografiske
Brug af kemisk grænseteknik til at skabe stål, der er stærkt og fleksibelt uden højt kulstofindh…Skematisk illustration af en PB, en GB, og en CB. (A) PB, en grænse mellem to korn af forskellig gittertype. (B) GB, en grænse mellem to korn af samme gittertype, men med forskellige krystallografiske -
 Befugtende ejendom af Li metal med grafitKontaktvinkeleksperimenter af Li-metal og grafitmaterialer:(a-c) stærkt orienteret pyrolytisk grafit (HOPG); (d-f) porøst carbonpapir (PCP); (g-i) lithieret porøst carbonpapir (litieret PCP). Kredit:©
Befugtende ejendom af Li metal med grafitKontaktvinkeleksperimenter af Li-metal og grafitmaterialer:(a-c) stærkt orienteret pyrolytisk grafit (HOPG); (d-f) porøst carbonpapir (PCP); (g-i) lithieret porøst carbonpapir (litieret PCP). Kredit:©
- Ingeniører viser, hvordan wolframoxid kan bruges som katalysator i bæredygtige kemiske omdannelser…
- Kvantematerialer:En ny stoftilstand med chirale egenskaber
- Akutte vinkler i den virkelige verden
- Kan en solflare forårsage en aurora borealis på jorden?
- Findes de fleste vand dybt under skorpen?
- Hvorfor astronauter lander på den mørke side af månen?


