Elektronkonfiguration af bor og dens ion?
bor (b)
* atomnummer: 5
* Elektronkonfiguration: 1S² 2S² 2P¹
Borion (b³⁺)
* opladning: +3
* Elektronkonfiguration: 1S²
Forklaring:
* bores neutrale atom: Bor har 5 elektroner, der distribueres i sine elektronskaller i henhold til Aufbau -princippet og Hunds regel.
* Den første skal (n =1) kan holde op til 2 elektroner, så den er fyldt med 1S².
* Den anden skal (n =2) kan holde op til 8 elektroner. Det starter med 2S², hvilket efterlader 1 elektron for at besætte en af 2p -orbitaler.
* Borion (b³⁺): Bor mister let sine 3 ydre elektroner (2S² 2P¹) for at opnå en stabil, tom ydre skal. Dette resulterer i en +3 ladning og en konfiguration, der er identisk med helium:1S².
 Varme artikler
Varme artikler
-
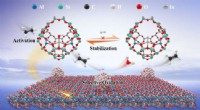 Forskere skræddersyer hovedgruppekatalysator med atomisk spredte In-steder til højeffektiv oxidati…Skematisk over det lokale koordinationsmiljø for isoleret In-sted og foreslået selektiv oxidativ dehydrogeneringsproces på hovedgruppe In-katalysator. Kredit:WANG Chaojie Overgangsmetaloxider er ka
Forskere skræddersyer hovedgruppekatalysator med atomisk spredte In-steder til højeffektiv oxidati…Skematisk over det lokale koordinationsmiljø for isoleret In-sted og foreslået selektiv oxidativ dehydrogeneringsproces på hovedgruppe In-katalysator. Kredit:WANG Chaojie Overgangsmetaloxider er ka -
 Kemikere skaber en ny vej til PHA'er:naturligt nedbrydeligt bioplastFra venstre:kandidatstuderende Andrea Westlie, professor Eugene Chen, og forsker Xiaoyan Tang i Chemistry Research Building. Kredit:John Eisele En bølge af offentlig fremdrift svulmer op mod krise
Kemikere skaber en ny vej til PHA'er:naturligt nedbrydeligt bioplastFra venstre:kandidatstuderende Andrea Westlie, professor Eugene Chen, og forsker Xiaoyan Tang i Chemistry Research Building. Kredit:John Eisele En bølge af offentlig fremdrift svulmer op mod krise -
 Forskere laver alkometer, der kan opdage marihuanaErvin Sejdic, PhD (til venstre) og Alexander Star, Ph.d., holde prototypen på deres THC-detekterende enhed op. Kredit:University of Pittsburgh Efterhånden som legalisering af rekreativ marihuana b
Forskere laver alkometer, der kan opdage marihuanaErvin Sejdic, PhD (til venstre) og Alexander Star, Ph.d., holde prototypen på deres THC-detekterende enhed op. Kredit:University of Pittsburgh Efterhånden som legalisering af rekreativ marihuana b -
 Kemikere bruger lys til at bygge biologisk aktive forbindelserSyntese af isoquinuclidiner ved hjælp af den blå LED-aktiverede fotokemi. Kredit:Jiajia Ma Nogle af de mest biologisk aktive molekyler, herunder syntetiske stoffer, indeholde en central, nitrogenh
Kemikere bruger lys til at bygge biologisk aktive forbindelserSyntese af isoquinuclidiner ved hjælp af den blå LED-aktiverede fotokemi. Kredit:Jiajia Ma Nogle af de mest biologisk aktive molekyler, herunder syntetiske stoffer, indeholde en central, nitrogenh
- Formes boraxkrystaller hurtigere end saltkrystaller?
- Hurtige bevægelige partikler og energi frigivet af ustabile kerner er former for?
- Hvilke organismer har gavn af forholdet mellem oksespætte og flodhest?
- Sådan laver du en 3-D Bohr Model
- Renere luft med geotermisk energi
- Forskere fanger, hvordan materialer går i stykker efter et ekstremt stød


