Hvad er den korrekte elektronkonfiguration af fosfor?
1S² 2S² 2p⁶ 3S² 3p³
Sådan forstår du det:
* fosfor (p) Har et atomnummer på 15, hvilket betyder, at det har 15 protoner og 15 elektroner.
* Elektronkonfiguration Beskriver arrangementet af elektroner i et atoms energiniveau og underniveauer.
* 1S²: Det første energiniveau (n =1) har et underskal, 'S' underskalet, der kan holde op til 2 elektroner.
* 2s²: Det andet energiniveau (n =2) har også et 'S' underskal, der holder 2 elektroner.
* 2p⁶: Det andet energiniveau har et 'P' underskal, der kan holde op til 6 elektroner.
* 3S²: Det tredje energiniveau (n =3) har et 's' underskal, der holder 2 elektroner.
* 3p³: Det tredje energiniveau har også et 'P' underskal, der indeholder 3 elektroner i fosfor.
Vigtig note: Mens dette er jordtilstands elektronkonfiguration, kan du også se fosforkonfiguration skrevet som [NE] 3S² 3P³ . Denne kortfattede notation bruger det tidligere ædle gaselement (neon, [NE]) til at repræsentere de fyldte indre skaller.
 Varme artikler
Varme artikler
-
 Autonom selvhelbredelse set i piezoelektriske molekylære krystallerKredit:CC0 Public Domain Et team af forskere fra Indian Institute of Science Education and Research i Kolkata, Indian Institute of Technology Kharagpur og RWTH Aachen University, har fundet en typ
Autonom selvhelbredelse set i piezoelektriske molekylære krystallerKredit:CC0 Public Domain Et team af forskere fra Indian Institute of Science Education and Research i Kolkata, Indian Institute of Technology Kharagpur og RWTH Aachen University, har fundet en typ -
 SwissFEL gør proteinstrukturer synligeMichael Hennig (til venstre) og Karol Nass på forsøgsstationen i SwissFEL, hvor deres pilotforsøg blev udført. Kredit:Paul Scherrer Institute/Mahir Dzambegovic Til udvikling af nye lægemidler, præ
SwissFEL gør proteinstrukturer synligeMichael Hennig (til venstre) og Karol Nass på forsøgsstationen i SwissFEL, hvor deres pilotforsøg blev udført. Kredit:Paul Scherrer Institute/Mahir Dzambegovic Til udvikling af nye lægemidler, præ -
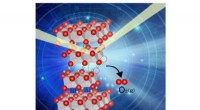 Forhindring af iltfrigivelse fører til sikrere batterier med høj energitæthedIltfrigivelse fra batterimaterialer, som kan forårsage termisk flugt. Kredit:Takashi Nakamura En forskergruppe har frembragt frisk indsigt om frigivelsen af ilt i lithium-ion-batterier, baner ve
Forhindring af iltfrigivelse fører til sikrere batterier med høj energitæthedIltfrigivelse fra batterimaterialer, som kan forårsage termisk flugt. Kredit:Takashi Nakamura En forskergruppe har frembragt frisk indsigt om frigivelsen af ilt i lithium-ion-batterier, baner ve -
 Lab afslører ny virkningsmekanisme mod SARS-CoV-2 af antiviralt lægemiddel remdesivir(Top) Den virale polymerase (blå oval) inkorporerer remdesivir (rød) i RNA-primerstrengen (grønne bobler) modsat uridin i skabelonen (gule/klare bobler). Et sammenstød mellem remdesivir og aminosyren
Lab afslører ny virkningsmekanisme mod SARS-CoV-2 af antiviralt lægemiddel remdesivir(Top) Den virale polymerase (blå oval) inkorporerer remdesivir (rød) i RNA-primerstrengen (grønne bobler) modsat uridin i skabelonen (gule/klare bobler). Et sammenstød mellem remdesivir og aminosyren
- NASA viser, at den største nedbør er fordrevet i tyfonen Chan-hom
- Hvilken grundfjeld ville mest sandsynligt indeholde fossiler?
- Hvornår er den største måneholdige?
- Kan en solflare potentielt ødelægge elektronik?
- Hvilket instrument vil du bruge til at finde flydende volumen?
- Forstå hvorfor BRCA2 er forbundet med kræftrisiko


