Hvad er valensen af svovl i MGSO4?
* Identificer gebyrerne for de andre ioner:
* Magnesium (mg) er i gruppe 2 i den periodiske tabel, så den har en +2 ladning (mg²⁺).
* Sulfat (SO₄) er en polyatomisk ion med en -2 ladning (SO₄²⁻).
* afbalancere anklagerne: Da ladningerne er ens og modsatte, annullerer de hinanden, hvilket resulterer i en neutral forbindelse (MGSO₄).
* Bestem valensen af svovl: I sulfationen er svovl (er) bundet til fire iltatomer (O). Hvert iltatom har en -2 -ladning, hvilket resulterer i en total negativ ladning på -8. For at afbalancere dette skal svovl have en +6 ladning.
Derfor er valensen af svovl i Mgso₄ +6.
 Varme artikler
Varme artikler
-
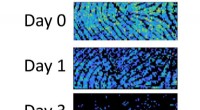 Rester i fingeraftryk indeholder spor af deres alderNiveauer af umættet triacylglycerol falder i fingeraftryk fra et individ fra dag 0 (øverst) til dag 1 (midten) og dag 3 (nederst). Kredit:Tilpasset fra Analytisk kemi 2020, DOI:10.1021/acs.analchem.
Rester i fingeraftryk indeholder spor af deres alderNiveauer af umættet triacylglycerol falder i fingeraftryk fra et individ fra dag 0 (øverst) til dag 1 (midten) og dag 3 (nederst). Kredit:Tilpasset fra Analytisk kemi 2020, DOI:10.1021/acs.analchem. -
 Bioluminescerende orm viste sig at have jern supermagterPergamentrørorm fanget i marken. Kredit:Dr. Evelien De Meulenaere, Scripps Institution of Oceanography ved UC San Diego. Forskere ved Scripps Institution of Oceanography ved University of Californ
Bioluminescerende orm viste sig at have jern supermagterPergamentrørorm fanget i marken. Kredit:Dr. Evelien De Meulenaere, Scripps Institution of Oceanography ved UC San Diego. Forskere ved Scripps Institution of Oceanography ved University of Californ -
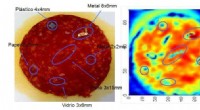 Design af sensorer til at detektere fremmedlegemer i fødevarerBillede opnået med denne teknologi, hvor der kan ses, på et stykke pølse, plast, metaller og splinter af glas i forskellige størrelser og former. Kredit:Elhuyar Fundazioa Forskere ved NUP/UPNA-Pub
Design af sensorer til at detektere fremmedlegemer i fødevarerBillede opnået med denne teknologi, hvor der kan ses, på et stykke pølse, plast, metaller og splinter af glas i forskellige størrelser og former. Kredit:Elhuyar Fundazioa Forskere ved NUP/UPNA-Pub -
 Sporing af atombevægelse i realtid mellem krystalkorn i metallerTing Zhu, professor i maskinteknik ved Georgia Tech, foran sine TEM-billeder af polykrystallinske metaller og en grafisk simulerende atomstruktur. Kredit:Georgia Tech Metalliske materialer, der bru
Sporing af atombevægelse i realtid mellem krystalkorn i metallerTing Zhu, professor i maskinteknik ved Georgia Tech, foran sine TEM-billeder af polykrystallinske metaller og en grafisk simulerende atomstruktur. Kredit:Georgia Tech Metalliske materialer, der bru


