Er mætning af benzen den samme for andre umættede hydrokarboner?
* Benzens unikke struktur: Benzen har en unik struktur med en ring med seks carbonatomer, der hver er bundet til et hydrogenatom. Elektronerne i carbon-carbonbindingerne delokaliseres og danner en stabil, plan ring. Denne delokalisering gør benzen usædvanligt stabil og resistent over for tilsætningsreaktioner, som er typiske for umættede kulbrinter.
* mætning vs. umættelse: Mætning henviser til antallet af hydrogenatomer, der kan tilsættes til et molekyle. Mættede kulbrinter har det maksimale mulige antal brintatomer, mens umættede carbonhydrider har færre.
* Benzenes aromatiske karakter: Benzens delokaliserede elektroner giver det en speciel egenskab kaldet "aromaticitet." Dette bidrager til dens stabilitet og unikke reaktivitet. Det gennemgår ikke let tilsætningsreaktioner som typiske alkener eller alkyner, som er de mest almindelige typer umættede kulbrinter.
Nøgleforskelle:
* Typiske umættede kulbrinter: Alkener og alkyner har dobbelt- eller tredobbelt bindinger, hvilket gør dem meget reaktive. De gennemgår let tilsætningsreaktioner, hvor dobbelt- eller tredobbeltbindingen er brudt, og der dannes nye enkeltbindinger.
* benzen: Benzen har et stabilt, delokaliseret ringsystem, der gør det mindre reaktivt end typiske umættede kulbrinter. Det foretrækker at gennemgå substitutionsreaktioner, hvor et hydrogenatom erstattes af et andet atom eller gruppe.
Kortfattet: Mens benzen betragtes som umættet på grund af dens ringstruktur, påvirker dens unikke aromatiske karakter signifikant dens reaktivitet og mætningsadfærd sammenlignet med andre umættede kulbrinter som alkener og alkyner.
 Varme artikler
Varme artikler
-
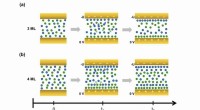 Forskere udvikler realtidsteknik til at studere ioniske væsker ved elektrodegrænsefladerTeamets forskning viste, at de ioniske rekonfigurationer, der forekommer nær guldelektroderne (gule stænger), afhænger af tykkelsen af de undersøgte ioniske flydende film, som illustreret i ovenståe
Forskere udvikler realtidsteknik til at studere ioniske væsker ved elektrodegrænsefladerTeamets forskning viste, at de ioniske rekonfigurationer, der forekommer nær guldelektroderne (gule stænger), afhænger af tykkelsen af de undersøgte ioniske flydende film, som illustreret i ovenståe -
 Biomarkører, der kan hjælpe med at bestemme, hvem der er i risiko for alvorlige COVID-19-symptomerKredit:Pixabay/CC0 Public Domain Et af de mange mysterier, der stadig omgiver COVID-19, er, hvorfor nogle mennesker kun oplever milde, influenzalignende symptomer, mens andre lider af livstruende
Biomarkører, der kan hjælpe med at bestemme, hvem der er i risiko for alvorlige COVID-19-symptomerKredit:Pixabay/CC0 Public Domain Et af de mange mysterier, der stadig omgiver COVID-19, er, hvorfor nogle mennesker kun oplever milde, influenzalignende symptomer, mens andre lider af livstruende -
 Vand, jordanalyseteknologi kan hjælpe med at forbedre oprydning og overvågning på forurenede Supe…Kredit:CC0 Public Domain Mindst 53 millioner amerikanere, inklusive omkring 18 procent af landets børn, bor mindre end tre miles fra en Superfund-side, ifølge Miljøstyrelsen. Kongressen oprettede
Vand, jordanalyseteknologi kan hjælpe med at forbedre oprydning og overvågning på forurenede Supe…Kredit:CC0 Public Domain Mindst 53 millioner amerikanere, inklusive omkring 18 procent af landets børn, bor mindre end tre miles fra en Superfund-side, ifølge Miljøstyrelsen. Kongressen oprettede -
 Lovende opdagelse kan føre til en bedre, billigere solcelleKredit:McGill University Forskere ved McGill University har fået spændende ny indsigt i perovskites egenskaber, et af verdens mest lovende materialer i jagten på at producere en mere effektiv, rob
Lovende opdagelse kan føre til en bedre, billigere solcelleKredit:McGill University Forskere ved McGill University har fået spændende ny indsigt i perovskites egenskaber, et af verdens mest lovende materialer i jagten på at producere en mere effektiv, rob


