Hvor mange atomer i 7,5 g natriumchlorid?
1. Find den molære masse af NaCl:
* Natrium (NA):22,99 g/mol
* Klor (CL):35,45 g/mol
* Molær masse af NaCl:22.99 + 35.45 =58.44 g/mol
2. Beregn antallet af mol NaCl:
* Mol =masse / molær masse
* Mol =7,5 g / 58,44 g / mol
* Mol ≈ 0,128 mol
3. Beregn antallet af formelenheder (NaCl -enheder):
* En mol af ethvert stof indeholder Avogadros antal partikler (6,022 x 10^23).
* Formelenheder på NaCl =0,128 mol * (6,022 x 10^23 Formelenheder/mol)
* Formelenheder på NaCl ≈ 7,71 x 10^22
4. Beregn det samlede antal atomer:
* Hver formelenhed af NaCl indeholder 1 natriumatom og 1 chloratom for i alt 2 atomer.
* Samlede atomer =7,71 x 10^22 Formelenheder * 2 Atomer/formelenhed
* Samlede atomer ≈ 1,54 x 10^23 atomer
Derfor er der ca. 1,54 x 10^23 atomer i 7,5 g natriumchlorid.
Sidste artikelHvorfor er formlen med merkurøst chlorid Hg2Cl2, men ikke HGCL?
Næste artikelHvad er ligningen for blygnitrat?
 Varme artikler
Varme artikler
-
 Forskere finder en måde at fremskynde DNA-overfladehybridiseringDen metode, vi har beskrevet, kan udvides til at undersøge intermolekylære kemiske reaktioner mellem en række enkeltmolekyler og kan føre til mekanistisk forståelse af kemiske reaktioner og udforsknin
Forskere finder en måde at fremskynde DNA-overfladehybridiseringDen metode, vi har beskrevet, kan udvides til at undersøge intermolekylære kemiske reaktioner mellem en række enkeltmolekyler og kan føre til mekanistisk forståelse af kemiske reaktioner og udforsknin -
 Et usandsynligt ægteskab blandt oxiderClaudia Cancellieri og Sebastian Siol undersøger heterostrukturelle legeringer på Empas Laboratory for Joining Technologies and Corrosion. Kredit:Swiss Federal Laboratories for Materials Science and T
Et usandsynligt ægteskab blandt oxiderClaudia Cancellieri og Sebastian Siol undersøger heterostrukturelle legeringer på Empas Laboratory for Joining Technologies and Corrosion. Kredit:Swiss Federal Laboratories for Materials Science and T -
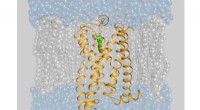 Farmakonutrition:Moderne lægemiddeldesign til funktionelle undersøgelserModel af den bitre receptor TAS2R14 med en af dens aktivatorer (ligander), flufenaminsyren. Kredit:Antonella Di Pizio/Leibniz-LSB@TUM Antonella Di Pizio og Maik Behrens fra Leibniz-instituttet f
Farmakonutrition:Moderne lægemiddeldesign til funktionelle undersøgelserModel af den bitre receptor TAS2R14 med en af dens aktivatorer (ligander), flufenaminsyren. Kredit:Antonella Di Pizio/Leibniz-LSB@TUM Antonella Di Pizio og Maik Behrens fra Leibniz-instituttet f -
 Ionledende polymer er afgørende for at forbedre neuromorfe enhederFotografi af en neuromorf enhed brugt i denne undersøgelse. Kredit:Shunsuke Yamamoto Neuromorf refererer til efterligning af adfærden hos hjernens neurale celler. Når man taler om neuromorfe compu
Ionledende polymer er afgørende for at forbedre neuromorfe enhederFotografi af en neuromorf enhed brugt i denne undersøgelse. Kredit:Shunsuke Yamamoto Neuromorf refererer til efterligning af adfærden hos hjernens neurale celler. Når man taler om neuromorfe compu
- Kan smartere skovbufferstrimler langs vandløb bidrage til at afbøde klimaændringer?
- Programmerbare transparente organiske selvlysende tags - skrivning med lys
- Nye lithium batterier fra brugte mobiltelefoner
- Sådan fungerer vandløse toiletter
- Hvordan at holde træer ved rydning af græsgange kan reducere klimakonsekvenserne
- Hvad er definitionen af nettofortrængning for fysik?


