Hvad er massen af opløst stof i 500 ml 0,341 m ammoniumchlorid?
1. Forstå udtrykkene:
* Molaritet (M): Mol opløst stof pr. Liter opløsning.
* opløst: Stoffet opløst i en opløsning.
* Løsning: En homogen blanding af opløst stof og opløsningsmiddel.
2. Beregn molen af opløst stof:
* Løsningsvolumen: 500 ml =0,5 L (siden 1 l =1000 ml)
* Molaritet: 0,341 m
* mol oplaking =molaritet x volumen (i liter)
* mol NH₄CL =0,341 M * 0,5 L =0,1705 mol
3. Beregn massen af opløst stof:
* Molær masse af NH₄CL: 14,01 g/mol (n) + 1,01 g/mol (H) x 4 + 35,45 g/mol (Cl) =53,49 g/mol
* masse af opløst stof =mol opløst x molær masse
* masse af NH₄CL =0,1705 mol * 53,49 g/mol =9,13 g
Derfor er massen af ammoniumchlorid (NH₄CL) i 500 ml af en 0,341 m opløsning 9,13 gram
Sidste artikelHvad er fusionsvarmen for natriumthiosulfatpentahydrat?
Næste artikelHvilke af disse er kemiske forbindelser O2 H2O CO2 N2?
 Varme artikler
Varme artikler
-
 Ionvindteknologiens gennembrud tager flugtenGennembrudsflyvning -- Adrian Ieta, fra SUNY Oswegos fakultet for elektro- og computeringeniør, og SUNY Research Foundation har ansøgt om patent på teknologi, der resulterede i en første af sin slags
Ionvindteknologiens gennembrud tager flugtenGennembrudsflyvning -- Adrian Ieta, fra SUNY Oswegos fakultet for elektro- og computeringeniør, og SUNY Research Foundation har ansøgt om patent på teknologi, der resulterede i en første af sin slags -
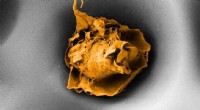 Hvorfor hviler makrofager i sundt vævEn makrofag i en pore, der måler 20 mikrometer på tværs (elektronmikroskopbillede). Kredit:ETH Zürich / Nikhil Jain og Isabel Gerber ETH -forskere har vist, at immunsystemets makrofager ikke kun r
Hvorfor hviler makrofager i sundt vævEn makrofag i en pore, der måler 20 mikrometer på tværs (elektronmikroskopbillede). Kredit:ETH Zürich / Nikhil Jain og Isabel Gerber ETH -forskere har vist, at immunsystemets makrofager ikke kun r -
 Ny opdagelse af en så stærk fotobase, det fortjener moniker af superEn ny opdagelse af en lysinduceret superfotobase ved Michigan State University afslører nogle af fotosyntesens ønskelige træk. Det tværfaglige team af forskere var i stand til at dokumentere den super
Ny opdagelse af en så stærk fotobase, det fortjener moniker af superEn ny opdagelse af en lysinduceret superfotobase ved Michigan State University afslører nogle af fotosyntesens ønskelige træk. Det tværfaglige team af forskere var i stand til at dokumentere den super -
 Forvandling af pollen til 3D-printblæk til biomedicinske applikationerDenne pollen-afledte blæk udviklet af NTU Singapore (i røret) er i stand til at holde sin form, når den afsættes på en overflade, gør det til et levedygtigt alternativ til nuværende blæk, der bruges t
Forvandling af pollen til 3D-printblæk til biomedicinske applikationerDenne pollen-afledte blæk udviklet af NTU Singapore (i røret) er i stand til at holde sin form, når den afsættes på en overflade, gør det til et levedygtigt alternativ til nuværende blæk, der bruges t
- Fifth Grade Ocean Floor Project
- Indlejring af etik i datalogi pensum
- Undersøgelse viser, at vores sol er mindre aktiv end lignende stjerner
- Musiksmag giver et vindue til, hvordan du tænker
- Spildevandsbehandlingssystem genvinder elektricitet, filtrerer vand
- Hvilket hårdt mineral vil mest sandsynligt overleve omfattende kemisk forvitring og danne sandkorn …


