Hvorfor opløses ethanol i vand og benzin?
Ethanol og vand:
* Hydrogenbinding: Ethanol har en hydroxylgruppe (-OH), som gør det muligt for den at danne hydrogenbindinger med vandmolekyler. Disse stærke bindinger er den primære årsag til ethanols opløselighed i vand.
* Polaritet: Ethanol er et polært molekyle på grund af elektronegativitetsforskellen mellem ilt og brint. Dette betyder, at det har en lidt positiv og lidt negativ ende, ligesom vand. Polære molekyler har en tendens til at opløses godt i andre polære opløsningsmidler.
Ethanol og benzin:
* ikke -polær karakter af benzin: Benzin består for det meste af kulbrinter, som er ikke -polære molekyler. Dette betyder, at der ikke er nogen signifikant tiltrækning mellem ethanols polære molekyler og de ikke -polære carbonhydridmolekyler i benzin.
* Begrænset blanding: Mens ethanol og benzin i nogen grad kan blandes, opløses de ikke rigtigt. De danner en heterogen blanding, hvilket betyder, at de forbliver separate faser.
Hvorfor forvirringen?
* gasohol: Nogle benzinblandinger indeholder en lille mængde ethanol (normalt 10%) for at forbedre forbrænding og reducere emissionerne. Dette kaldes Gasohol. Den begrænsede opløselighed af ethanol i benzin giver mulighed for denne blanding, men det er vigtigt at bemærke, at de ikke er fuldt blandbare.
* Misforståelser: Udtrykkene "opløses" og "mix" bruges undertiden om hverandre, hvilket fører til forvirring. Ethanol og benzin kan blande, men de opløses ikke på samme måde som ethanol opløses i vand.
Kortfattet:
Ethanol opløses i vand på grund af stærk hydrogenbinding og lignende polariteter. Det blandes, men opløses ikke rigtigt i benzin på grund af den ikke -polære karakter af benzin og den begrænsede attraktion mellem molekylerne.
 Varme artikler
Varme artikler
-
 Team sikrer stabilitet af afsaltningsprocessen med magnesiumForsker Hye-Won Kim tilføjer magnesium til havvand for at hæmme tilsmudsning af afsaltningsmembraner. Kredit:Korea Institute of Science and Technology (KIST) Et koreansk forskerhold fandt en metod
Team sikrer stabilitet af afsaltningsprocessen med magnesiumForsker Hye-Won Kim tilføjer magnesium til havvand for at hæmme tilsmudsning af afsaltningsmembraner. Kredit:Korea Institute of Science and Technology (KIST) Et koreansk forskerhold fandt en metod -
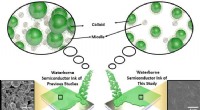 Miljøvenlig vandbåren halvlederblæk ved hjælp af overfladeaktivt stofSammenligning af den vandbårne halvlederblæk i denne undersøgelse og den i de tidligere undersøgelser. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Et forskerhold fra Energy
Miljøvenlig vandbåren halvlederblæk ved hjælp af overfladeaktivt stofSammenligning af den vandbårne halvlederblæk i denne undersøgelse og den i de tidligere undersøgelser. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Et forskerhold fra Energy -
 En ny løsning til spildevandsrensningKredit:Pixabay/CC0 Public Domain Syntetiske farvestoffer bruges på tværs af en lang række industrier og udgør en alvorlig bekymring, når det kommer til vandforurening. Disse farvestoffer er ikke ku
En ny løsning til spildevandsrensningKredit:Pixabay/CC0 Public Domain Syntetiske farvestoffer bruges på tværs af en lang række industrier og udgør en alvorlig bekymring, når det kommer til vandforurening. Disse farvestoffer er ikke ku -
 Forskere får en vigtig kemisk forbindelseMetalcarbonylkompleks fyldt i en flaske. Kredit:AG Krossing/J. Bohnenberger Siden opdagelsen af det første homoleptiske metalcarbonylkompleks Ni(CO) 4 for mere end 130 år siden, forskere forsø
Forskere får en vigtig kemisk forbindelseMetalcarbonylkompleks fyldt i en flaske. Kredit:AG Krossing/J. Bohnenberger Siden opdagelsen af det første homoleptiske metalcarbonylkompleks Ni(CO) 4 for mere end 130 år siden, forskere forsø
- Forklar, hvorfor de fleste kulstofforbindelser klassificeres som organiske forbindelser?
- Forskere udvikler bedre måder at dyrke levende hjerteceller på på den internationale rumstation
- BP nåede en hyggelig løsning med Mexico om Deepwater-udslip:vagthund
- Hvilken slags elektromagnetisk stråling kunne bruges til at se molekyler?
- Hvad er fraktionsmanipulativer?
- Programmering af pH:Ny teknik kan fremskynde DNA-syntese


