Forbindelse, der danner hydroxidioner i opløsning?
Her er nogle eksempler:
* metalhydroxider: Dette er ioniske forbindelser, der indeholder en metalkation og hydroxidanionen (OH-). Eksempler inkluderer natriumhydroxid (NaOH), kaliumhydroxid (KOH) og calciumhydroxid (Ca (OH) 2).
* Nogle ikke-metaloxider: Visse ikke-metaloxider reagerer med vand for at danne syrer, som derefter frigiver hydroxidioner. For eksempel reagerer svovldioxid (SO2) med vand til dannelse af svovlsyre (H2SO3), som derefter frigiver hydroxidioner.
* ammoniumhydroxid (NH4OH): Selvom det ikke er et ægte hydroxid, er ammoniumhydroxid en svag base, der danner ammoniumioner (NH4+) og hydroxidioner (OH-) i opløsning.
En forbindelse til at danne hydroxidioner i opløsning er det, der gør det til en base. Baser er kendetegnet ved deres glatte fornemmelse, bitter smag og evne til at neutralisere syrer.
Sidste artikelHvad er den afbalancerede ligning af svovldioxid plus vand?
Næste artikelHvilke ioner er til stede cæsiumcarbonat?
 Varme artikler
Varme artikler
-
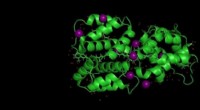 Vores første kig på et nyt lysabsorberende protein i cyanobakterierKredit:Michigan State University Cyanobakterier er små, hårdføre organismer. Hver celle er 25 gange mindre end et menneskehår, men lad ikke størrelsen narre dig. Deres kollektive evne til at udvid
Vores første kig på et nyt lysabsorberende protein i cyanobakterierKredit:Michigan State University Cyanobakterier er små, hårdføre organismer. Hver celle er 25 gange mindre end et menneskehår, men lad ikke størrelsen narre dig. Deres kollektive evne til at udvid -
 En strømlinet tilgang til bestemmelse af termiske egenskaber for krystallinske faste stoffer og leg…Et neuralt netværk, der bærer fuld krystal -symmetri, muliggør effektiv træning af krystallinske faste stoffer. Kredit:Massachusetts Institute of Technology I et essay i september 2020 i Naturene
En strømlinet tilgang til bestemmelse af termiske egenskaber for krystallinske faste stoffer og leg…Et neuralt netværk, der bærer fuld krystal -symmetri, muliggør effektiv træning af krystallinske faste stoffer. Kredit:Massachusetts Institute of Technology I et essay i september 2020 i Naturene -
 Maling med halvlederePerovskite portræt af Marie Skłodowska-Curie. Kredit:Lukas Helmbrecht AMOLF-forskerne Lukas Helmbrecht og Wim Noorduin har udviklet en reaktiv blæk, der kan males på et lige så reaktivt lærred. Bl
Maling med halvlederePerovskite portræt af Marie Skłodowska-Curie. Kredit:Lukas Helmbrecht AMOLF-forskerne Lukas Helmbrecht og Wim Noorduin har udviklet en reaktiv blæk, der kan males på et lige så reaktivt lærred. Bl -
 Nyt hardcarbonanodemateriale til natriumionbatterier løser litiumproblemetDen nye kapacitet af dette nye hårde kulstofelektrodemateriale betyder, at en 19% stigning i energitæthed i vægt er mulig i natriumionbatterier sammenlignet med lithium-ion-batterier Kredit:Shinichi K
Nyt hardcarbonanodemateriale til natriumionbatterier løser litiumproblemetDen nye kapacitet af dette nye hårde kulstofelektrodemateriale betyder, at en 19% stigning i energitæthed i vægt er mulig i natriumionbatterier sammenlignet med lithium-ion-batterier Kredit:Shinichi K
- Hvorfor er planeter næsten sfæriske?
- Kriminalitetsbekæmpelse er lige blevet nemmere, efterhånden som indbrudstyve afslører alt
- Hvor kommer de fleste af energien i jordens atmosfærer og oceaner levende systemer fra?
- Hvor mødes jordplader?
- Hvilken type kollision konserveres kinetisk energi?
- Galaktisk vindkvælende stjernedannelse er den fjerneste hidtil set


