Hvad er reaktionen, når ammoniumsulfit sættes i vand?
(NH₄) ₂SO₃ (S) → 2NH₄⁺ (AQ) + SO₃²⁻ (AQ)
Her er en sammenbrud:
* (NH₄) ₂SO₃ (S): Ammoniumsulfit i sin faste tilstand.
* 2nh₄⁺ (aq): To ammoniumioner (NH₄⁺) opløst i vand.
* so₃²⁻ (aq): En sulfition (SO₃²⁻) opløst i vand.
Reaktionen er reversibel hvilket betyder, at de opløste ioner også kan rekombineres for at danne fast ammoniumsulfit igen, hvis vandet fordampes. Denne proces kaldes opløselighed ligevægt .
Det er vigtigt at bemærke, at ammoniumsulfit er en svag base . Dette betyder, at sulfitionen (SO₃²⁻) kan reagere med vand i lille grad, hvilket producerer nogle hydroxidioner (OH⁻) og gør opløsningen lidt grundlæggende. Den samlede reaktion er imidlertid primært opløsning og dissociation.
Sidste artikelHvorfor reagerer brom ikke med vandigt kaliumchlorid?
Næste artikelHvad er der ved type kemisk vejrforhold?
 Varme artikler
Varme artikler
-
 En hurtig, effektiv COVID-19-biosensor er under udviklingRajesh Sardar, center, taler med Omolade Olofintuyi, venstre, en bachelor fra Howard University, som forskede i en avanceret biosensor for COVID-19 i sit laboratorium denne sommer gennem et NSF-finans
En hurtig, effektiv COVID-19-biosensor er under udviklingRajesh Sardar, center, taler med Omolade Olofintuyi, venstre, en bachelor fra Howard University, som forskede i en avanceret biosensor for COVID-19 i sit laboratorium denne sommer gennem et NSF-finans -
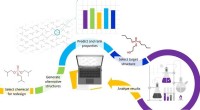 Sådan designes sikre og bæredygtige kemikalierMetode præsenteret af forskerne. Som et casestudie genererede de over seks millioner alternativer til en populær flammehæmmer og evaluerede deres egenskaber. Kredit:UvA/HIMS Med mange menneskeskabt
Sådan designes sikre og bæredygtige kemikalierMetode præsenteret af forskerne. Som et casestudie genererede de over seks millioner alternativer til en populær flammehæmmer og evaluerede deres egenskaber. Kredit:UvA/HIMS Med mange menneskeskabt -
 Smart kemi fjerner kræftbekæmpende lægemidler med alvorlige bivirkningerKredit:CC0 Public Domain Forskere fra Leiden University Medical Center (LUMC) og Leiden Institute of Chemistry har gjort en vigtig opdagelse om det almindeligt anvendte kræftbekæmpende stof doxoru
Smart kemi fjerner kræftbekæmpende lægemidler med alvorlige bivirkningerKredit:CC0 Public Domain Forskere fra Leiden University Medical Center (LUMC) og Leiden Institute of Chemistry har gjort en vigtig opdagelse om det almindeligt anvendte kræftbekæmpende stof doxoru -
 Svampeproduceret pigment viser løfte som halvledermaterialeKredit:Oregon State University Forskere ved Oregon State University ser på et meget holdbart organisk pigment, brugt af mennesker i kunstværker i hundredvis af år, som en lovende mulighed som halv
Svampeproduceret pigment viser løfte som halvledermaterialeKredit:Oregon State University Forskere ved Oregon State University ser på et meget holdbart organisk pigment, brugt af mennesker i kunstværker i hundredvis af år, som en lovende mulighed som halv
- Hvordan man manipulerer lys på nanoskalaen over brede frekvensområder
- NASA-billeder afslører de stærkeste områder af Tropical Storm Beta
- Hvorfor har forskere brug for at klassificere levende organismer?
- Hvorfor modificerede carbon nanorør kan hjælpe med reproducerbarhedsproblemet
- Eksotiske elektron-elektron-interaktioner fundet unødvendige for ledning i nikkelater
- Hvorfor er energien vigtig?


