Hvad er formlen for hexaaquacobalt II -klorid?
Sådan nedbrydes det:
* [CO (H₂O) ₆] ²⁺: Dette er den komplekse ion.
* co²⁺: Cobalt (II) ion. Det romerske tal II angiver, at koboltionen har en +2 ladning.
* (H₂O) ₆: Seks vandmolekyler koordineres til kobolt (II) -ionen, der fungerer som ligander.
* [] ²⁺: Hele kompleksionen har en +2 ladning for at afbalancere +2 ladning af koboltionen.
* cl⁻: Chloridion.
* [CO (H₂O) ₆] Cl₂: Den komplette formel kombinerer den komplekse ion og to chloridioner for at opnå en neutral forbindelse.
Sidste artikelHvilken frigivelse hydroxidioner, når det opløses i vand?
Næste artikelHvorfor klassificeres kulstof og kobber som elementer?
 Varme artikler
Varme artikler
-
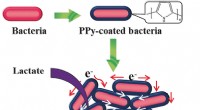 Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s
Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s -
 De smukkeste solceller er inspireret af naturenVi tror på, at disse solceller har en fremtid, og kemien er utrolig spændende, ” siger Audun Formo Buene. Kredit:Per Henning, NTNU Organiske solceller er normalt mindre effektive end siliciumsolce
De smukkeste solceller er inspireret af naturenVi tror på, at disse solceller har en fremtid, og kemien er utrolig spændende, ” siger Audun Formo Buene. Kredit:Per Henning, NTNU Organiske solceller er normalt mindre effektive end siliciumsolce -
 Små oplyste stregkoder identificerer molekyler ved deres blinkDisse små lyspunkter kan ligne stjerner, der blinker på himlen. Men i virkeligheden er de forskellige molekyler af oplyst DNA, blinker til og fra, mens de binder og afbinder under et mikroskop. Kredit
Små oplyste stregkoder identificerer molekyler ved deres blinkDisse små lyspunkter kan ligne stjerner, der blinker på himlen. Men i virkeligheden er de forskellige molekyler af oplyst DNA, blinker til og fra, mens de binder og afbinder under et mikroskop. Kredit -
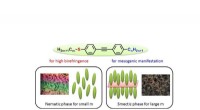 Svovl forbedrer dobbeltbrydningen til udvikling af flydende krystallinske molekylerBilleder af alkylthiogruppestavlignende molekyler, der udviser flydende krystallinitet ved stuetemperatur, og fasestrukturerne. Kredit:Toyohashi University of Technology Et team af forskere ledet
Svovl forbedrer dobbeltbrydningen til udvikling af flydende krystallinske molekylerBilleder af alkylthiogruppestavlignende molekyler, der udviser flydende krystallinitet ved stuetemperatur, og fasestrukturerne. Kredit:Toyohashi University of Technology Et team af forskere ledet
- Hvilke to energitransformationer, der forekommer i et vandkraftværk?
- Struktur, der holder hvert kromosom til sin nøjagtige kopi?
- Hvorfor forekommer solformørkelse kun på New Moon -dage?
- Hvorfor er der en cirkel omkring månen i aften?
- Hvad bruges maskiner til?
- Broadcaster opfordrer fodboldmyndighederne til ikke at overlade markedet til kriminelle


