Hvad er formen på H2O2?
Her er en sammenbrud:
* det centrale iltatom: De to iltatomer er forbundet med en enkelt binding, og hver har to ensomme par elektroner.
* Hydrogenatomerne: Hvert hydrogenatom er bundet til et af iltatomerne.
* den dihedrale vinkel: De to planer, der er defineret af H-O-O-H-atomerne, er ikke perfekt på linje. I stedet danner de en let snoet, ikke-plane struktur.
Hvorfor er det ikke-plan?
Den ikke-plane struktur skyldes de frastødende kræfter mellem de ensomme par elektroner på iltatomerne. Disse kræfter skubber brintatomerne lidt ud af planet, hvilket resulterer i den snoede, åbne bogform.
Her er en visuel analogi:Forestil dig at åbne en bog lidt. De to sider er ikke perfekt flade, men de er let vippede. Dette svarer til strukturen af hydrogenperoxid.
Bemærk: Selvom strukturen ofte er repræsenteret som en plan struktur i lærebøger, er det vigtigt at huske, at det faktisk er ikke-plan.
Sidste artikelHvordan annealer du et jernholdigt metal?
Næste artikelEr ammoniak en stærk syre eller base?
 Varme artikler
Varme artikler
-
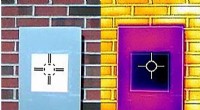 Den hvideste maling er her - og den er den sejeste. Bogstaveligt talt.Et infrarødt kamera viser, hvordan en prøve af den hvideste hvide maling (den mørke lilla firkant i midten) faktisk afkøler brættet under omgivelsestemperatur, noget, som ikke engang kommercielle varm
Den hvideste maling er her - og den er den sejeste. Bogstaveligt talt.Et infrarødt kamera viser, hvordan en prøve af den hvideste hvide maling (den mørke lilla firkant i midten) faktisk afkøler brættet under omgivelsestemperatur, noget, som ikke engang kommercielle varm -
 En studerendes mission for at beskytte verdens mest værdifulde ressourceHavvandsafsaltning ved hjælp af membranprocesser. Kredit:Johnson Effoe Efome Hooman Chamani, en ph.d. kandidat i Ottawa, er motiveret af én ting:At løse den globale vandkrise på en miljøvenlig måd
En studerendes mission for at beskytte verdens mest værdifulde ressourceHavvandsafsaltning ved hjælp af membranprocesser. Kredit:Johnson Effoe Efome Hooman Chamani, en ph.d. kandidat i Ottawa, er motiveret af én ting:At løse den globale vandkrise på en miljøvenlig måd -
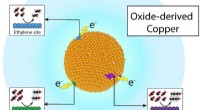 Kulbrændstoffer bliver grønne for vedvarende energiForskere ved Berkeley Lab og Joint Center for Artificial Photosynthesis har vist, at genanvendelse af kuldioxid til værdifulde kemikalier, såsom ethylen og propanol, og brændstoffer som ethanol, kan v
Kulbrændstoffer bliver grønne for vedvarende energiForskere ved Berkeley Lab og Joint Center for Artificial Photosynthesis har vist, at genanvendelse af kuldioxid til værdifulde kemikalier, såsom ethylen og propanol, og brændstoffer som ethanol, kan v -
 Sensoren registrerer lugt af dårlig åndeKredit:American Chemical Society Har du nogensinde ønsket, at du kunne lave et hurtigt åndedrætstjek før et vigtigt møde eller en stor date? Nu forskere, rapportering i ACS journal Analytisk kemi
Sensoren registrerer lugt af dårlig åndeKredit:American Chemical Society Har du nogensinde ønsket, at du kunne lave et hurtigt åndedrætstjek før et vigtigt møde eller en stor date? Nu forskere, rapportering i ACS journal Analytisk kemi
- Hvorfor var det ikke så langt side af månen var ukendt indtil 1959?
- Hvad er energitransformationen i bøjning af metal frem og tilbage, indtil det bliver varmt?
- Sådan opløses EDTA i Water
- Ramanujan-maskine genererer automatisk formodninger for fundamentale konstanter
- Hvordan anvendes fysik i madlavning?
- Spinat:Kemiforsøg viser potentiale til at drive brændselsceller


