Hvorfor gennemgår phenol trisubstitution i vandig bromopløsning?
1. Aktivering af ringen: Hydroxylgruppen (-OH) fastgjort til benzenringen i phenol er en elektron-donerende gruppe. Det øger elektrondensiteten i ringen, især ved ortho- og para -positionerne. Dette gør ringen mere modtagelig for elektrofilt angreb.
2. Dannelse af en resonans stabiliseret mellemprodukt: Når brom reagerer med phenol, danner den et bromoniumion -mellemprodukt. Dette mellemprodukt stabiliseres af resonans med det ensomme par elektroner på oxygenatomet i hydroxylgruppen. Denne resonansstabilisering gør reaktionen mere gunstig.
3. Elektrofilt angreb: Bromoniumionen, der er en stærk elektrofil, angriber let de elektronrige ortho- og para-positioner i phenolringen. Den første bromatom går ind i en af disse positioner og aktiverer yderligere ringen mod elektrofilt angreb.
4. på hinanden følgende bromering: Efter den første bromering bliver ringen endnu mere aktiveret på grund af tilstedeværelsen af bromsubstituenten. Dette gør det muligt at introduceres, at de anden og tredje bromatomer indføres i ortho- og para -positionerne, hvilket fører til trisubstitution.
5. Vand som opløsningsmiddel: Vand, der er et polært opløsningsmiddel, hjælper med at stabilisere de mellemliggende carbocations dannet under reaktionen. Dette fremmer reaktionen yderligere.
Generelt gør kombinationen af den elektron-donerende virkning af hydroxylgruppen, resonansstabiliseringen af mellemproduktet og tilstedeværelsen af vand som opløsningsmiddel phenol meget modtagelig for trisubstitution i vandig bromopløsning.
Det er vigtigt at bemærke, at reaktionen kan kontrolleres for at opnå mono- eller di-bromerede produkter ved at justere reaktionsbetingelserne. For eksempel kan anvendelse af en kold opløsning af brom i et ikke-polært opløsningsmiddel som carbontetrachlorid føre til mono-bromination.
Sidste artikelHvor mange orbitaler har zink?
Næste artikelHvilket stof fremstilles, når kalksten og ler opvarmes sammen?
 Varme artikler
Varme artikler
-
 Evergreen idé gør biomasse-DNA til nedbrydelige materialerKredit:CC0 Public Domain DNA har mange praktiske anvendelser. Det gemmer blueprintet af genetisk kode. Det hjælper med at indlede arternes udvikling. Det kan også potentielt gøre en stærkere, mer
Evergreen idé gør biomasse-DNA til nedbrydelige materialerKredit:CC0 Public Domain DNA har mange praktiske anvendelser. Det gemmer blueprintet af genetisk kode. Det hjælper med at indlede arternes udvikling. Det kan også potentielt gøre en stærkere, mer -
 Hurtig test for at sikre høj mælkekvalitetChip med integreret lyskilde og lysdetektor til analyse af forurenende stoffer i mælk. Kredit:Fraunhofer-Gesellschaft Standarder for fødevaresikkerhed og fødevarekvalitet har aldrig været højere i
Hurtig test for at sikre høj mælkekvalitetChip med integreret lyskilde og lysdetektor til analyse af forurenende stoffer i mælk. Kredit:Fraunhofer-Gesellschaft Standarder for fødevaresikkerhed og fødevarekvalitet har aldrig været højere i -
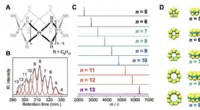 En forberedende reaktion ved hjælp af platinklynger med en encifret atomicitet realiseretFigur (A) viser kompleksernes kemiske struktur, (B) viser kromatogrammet for HPLC -adskillelsen med størrelsesekskluderingskolonner, (C) viser MALDI-TOF-massespektre for de isolerede platinkomplekser
En forberedende reaktion ved hjælp af platinklynger med en encifret atomicitet realiseretFigur (A) viser kompleksernes kemiske struktur, (B) viser kromatogrammet for HPLC -adskillelsen med størrelsesekskluderingskolonner, (C) viser MALDI-TOF-massespektre for de isolerede platinkomplekser -
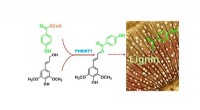 Forskere ID -enzym til fremstilling af nøgleindustrielt kemikalie i planterBrookhaven Lab-forskere identificerede et enzym (PHBMT1), der overfører p-hydoxybenzoat (grønt) til lignin-byggesten i poppel. Det resulterende konjugat inkorporeres derefter i den spirende ligninpoly
Forskere ID -enzym til fremstilling af nøgleindustrielt kemikalie i planterBrookhaven Lab-forskere identificerede et enzym (PHBMT1), der overfører p-hydoxybenzoat (grønt) til lignin-byggesten i poppel. Det resulterende konjugat inkorporeres derefter i den spirende ligninpoly
- Hvilke tre forskellige måder, hvorpå energi kan opbevares som stammeenergi?
- Hvilken underspecialitet af jordvidenskab studerer gamle miljøer?
- Rumfartøjs deorbiterende enhed klar til kommende testlancering
- Er solen den mindste stjerne sammenlignet med andre?
- Hvilke slags ændringer forekommer som en luftmasse bevæger sig over området?
- Hvilken type kemisk gruppering til stede i alle proteiner?


