Hjælp mig med at finde valensen af dichromat ammoniumdichromat?
1. Dichromate ion (cr₂o₇²⁻)
* krom (CR): Krom har typisk en valens på +3 eller +6. I dichromationen har den en valens på +6.
* ilt (O): Oxygen har altid en valens på -2.
* Find dichromatens valency:
* Lad dikromationens valens være x.
* Vi har 2 Cr-atomer (+6 hver) og 7 O-atomer (-2 hver).
* Ligningen er:2 (+6) + 7 (-2) =x
* Løsning af dette giver os x =-2. Derfor er dichromationens valens -ion -2.
2. Ammoniumdichromat ((nh₄) ₂cr₂o₇)
* ammoniumion (NH₄⁺): Ammonium har en valens på +1.
* dichromate ion (cr₂o₇²⁻): Som vi etablerede tidligere, har dette en valens på -2.
* Find valensen af ammoniumdichromat:
* Forbindelsen er neutral, hvilket betyder, at summen af valenserne skal være nul.
* Der er to ammoniumioner (+1 hver) og en dichromation (-2).
* Ligningen er:2 (+1) + (-2) =0
* Dette bekræfter forbindelsens neutralitet.
Nøglepunkter:
* Valency er den kombinerende kraft af et element eller ion.
* I ioniske forbindelser skal ionens valenser afbalancere for at skabe en neutral forbindelse.
Fortæl mig, hvis du har flere spørgsmål om valens eller andre kemiske koncepter!
Sidste artikelHvad er formlen for ammoniumchromat?
Næste artikelHvad er formlen, når flydende hydrogenperoxid nedbrydes til vand og iltgas?
 Varme artikler
Varme artikler
-
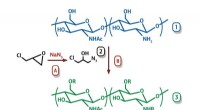 Kemikere får nyt materiale til antibakterielle madbelægningerRUDN University kemikere har udviklet en enkel og bekvem metode til fremstilling af derivater af den naturlige polymer chitosan. Disse derivater er ugiftige og har en udtalt antibakteriel aktivitet på
Kemikere får nyt materiale til antibakterielle madbelægningerRUDN University kemikere har udviklet en enkel og bekvem metode til fremstilling af derivater af den naturlige polymer chitosan. Disse derivater er ugiftige og har en udtalt antibakteriel aktivitet på -
 Hurtig måling af aerosolens volatilitet ved hjælp af et deep learning-baseret bærbart mikroskopEn mobil og omkostningseffektiv enhed er designet til at måle flygtigheden af partikler ved hjælp af deep learning. Kredit:Ozcan Lab, UCLA. Eksponering for partikler (PM) har været forbundet med
Hurtig måling af aerosolens volatilitet ved hjælp af et deep learning-baseret bærbart mikroskopEn mobil og omkostningseffektiv enhed er designet til at måle flygtigheden af partikler ved hjælp af deep learning. Kredit:Ozcan Lab, UCLA. Eksponering for partikler (PM) har været forbundet med -
 Forskeren udvikler bæredygtigt grønt te-baseret læderalternativDenne prototype af den grønne te-materialebaserede sko er et bæredygtigt alternativ til lædersko. Det blev skabt af Auburn-forskeren Young-A Lee. Kredit:Auburn University i Montgomery En global be
Forskeren udvikler bæredygtigt grønt te-baseret læderalternativDenne prototype af den grønne te-materialebaserede sko er et bæredygtigt alternativ til lædersko. Det blev skabt af Auburn-forskeren Young-A Lee. Kredit:Auburn University i Montgomery En global be -
 Ny strategi for levering af terapeutiske proteiner kan hjælpe med at behandle degenerative øjensyg…Kredit:Unsplash/CC0 Public Domain Et forskningshold fra University of Toronto Engineering har skabt en ny platform, der leverer flere terapeutiske proteiner til kroppen, hver med sin egen uafhængig
Ny strategi for levering af terapeutiske proteiner kan hjælpe med at behandle degenerative øjensyg…Kredit:Unsplash/CC0 Public Domain Et forskningshold fra University of Toronto Engineering har skabt en ny platform, der leverer flere terapeutiske proteiner til kroppen, hver med sin egen uafhængig
- Når lys fra en stjerne når jorden er den stadig der?
- Ingeniører opdager balancegang i nanoskala, der afspejler kræfter, der arbejder i levende systemer
- Er knogler en fast væske eller gas?
- Fysikere skaber første direkte billeder af firkanten af bølgefunktionen af et brintmolekyle
- Forskere finder, at forskellige samfund omfatter bakteriemåtter, der truer koralrev
- Metalliske nanopartikler hjælper med at bestemme procentdelen af flygtige forbindelser


