Hvordan finder du gebyret for nitrogen?
1. Elementært nitrogen:
* I sin elementære tilstand (N₂) eksisterer nitrogen som et diatomisk molekyle. Hvert nitrogenatom har uden gebyr (neutral).
2. Ioner:
* Nitrogen kan danne ioner med en negativ ladning. Den mest almindelige ion er nitrid (n³⁻) , som har en gebyr på -3. Dette skyldes, at nitrogen har brug for yderligere tre elektroner for at opnå en stabil octet -konfiguration.
3. Forbindelser:
* I forbindelser kan nitrogen have forskellige ladninger afhængigt af de andre atomer, det er bundet til.
* For at bestemme gebyret for nitrogen i en forbindelse kan du bruge følgende regler:
* Summen af ladningerne i en neutral forbindelse skal være lig med nul.
* Anklagen for en monatomisk ion er lig med dets gruppenummer minus 18.
Eksempel:
Lad os tage eksemplet på ammoniak (NH₃):
* Hydrogen (H) har en afgift på +1.
* Forbindelsen er neutral.
* Derfor skal ladningen af nitrogen (N) være -3 for at afbalancere +3 ladning fra de tre hydrogenatomer.
4. Oxidation siger:
* Oxidationstilstande er en måde at repræsentere den tilsyneladende ladning af et atom i en forbindelse, men de repræsenterer ikke nødvendigvis den faktiske ladning.
* Nitrogen kan have oxidationstilstande, der spænder fra -3 til +5.
Nøglepunkter:
* Anklagen for nitrogen afhænger af dets kemiske miljø.
* I sin elementære tilstand har nitrogen ingen gebyr.
* Nitrogen danner ofte nitridionen (n³⁻).
* I forbindelser kan ladningen af nitrogen bestemmes ved hjælp af ladningsbalanceringsregler.
Hvis du giver mig en bestemt forbindelse eller situation, kan jeg hjælpe dig med at bestemme gebyret for nitrogen i dette tilfælde.
Sidste artikelHvilket element har flere protoner end klor, men færre kalium?
Næste artikelBinær ionisk sammensat navn til CO2O3?
 Varme artikler
Varme artikler
-
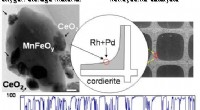 Ny katalysatorkomposit reducerer brugen af sjældne jordarterEn nyudviklet katalysator fra Japan, CeO2/MnFeOy, har både hurtig frigivelse og store opbevaringsmuligheder for ilt. Dens høje ydeevne i konverteringshastigheden af NOx, CO, og total kulbrinte til m
Ny katalysatorkomposit reducerer brugen af sjældne jordarterEn nyudviklet katalysator fra Japan, CeO2/MnFeOy, har både hurtig frigivelse og store opbevaringsmuligheder for ilt. Dens høje ydeevne i konverteringshastigheden af NOx, CO, og total kulbrinte til m -
 Laboratoriegennembrud inden for 3-D print af glasEn ny 3D-printteknik, udviklet hos Lawrence Livermore, kunne tillade videnskabsmænd at udskrive glas, der inkorporerer forskellige brydningsindekser i en enkelt flad optik, gør efterbehandling billige
Laboratoriegennembrud inden for 3-D print af glasEn ny 3D-printteknik, udviklet hos Lawrence Livermore, kunne tillade videnskabsmænd at udskrive glas, der inkorporerer forskellige brydningsindekser i en enkelt flad optik, gør efterbehandling billige -
 Bæredygtig vandkvalitetssensor lavet af menneskehår-afledte kulstofprikkerKredit:CC0 Public Domain Griffith University-forskere har brugt menneskehåraffald til at udvikle bæredygtige organiske højteknologiske enheder til vandkvalitetstest af forurenende stoffer. Profes
Bæredygtig vandkvalitetssensor lavet af menneskehår-afledte kulstofprikkerKredit:CC0 Public Domain Griffith University-forskere har brugt menneskehåraffald til at udvikle bæredygtige organiske højteknologiske enheder til vandkvalitetstest af forurenende stoffer. Profes -
 En intelligent, formformende, selvhelbredende materiale til integreret kunstig muskel og nervevævForskere udvikler et formformende materiale med en hidtil uset multifunktionalitet til blød robotik og bærbar elektronik. Kredit:Soft Machines Lab, Carnegie Mellon University Fremskridt inden for
En intelligent, formformende, selvhelbredende materiale til integreret kunstig muskel og nervevævForskere udvikler et formformende materiale med en hidtil uset multifunktionalitet til blød robotik og bærbar elektronik. Kredit:Soft Machines Lab, Carnegie Mellon University Fremskridt inden for
- Hvad er de to mest rigelige forbindelser i atmosfæren?
- Hvad er de modstrømsudvekslingssystemer i dyresystemer?
- Hvorfor er zebramuslinger så klistrede? Undersøgelse kan føre til nye industrielle belægninger, …
- Hvilke betingelser kræves for en solcellypse?
- Hvad skal kernekraftværker med energi?
- Hvilken moderne branchevidenskab var alkymi forløberen?


