Hvilken forbindelse ville kulstof og fluor sandsynligvis dannes?
* Valenselektroner: Carbon har 4 valenselektroner og fluor har 7 valenselektroner. Carbon skal få 4 elektroner for at opnå en stabil oktet, mens fluor skal få 1 elektron.
* ionisk binding: Carbon og fluor har en betydelig forskel på elektronegativitet, hvilket antyder ionisk binding. Forskellen er imidlertid ikke stor nok til at danne en rent ionisk forbindelse.
* kovalent binding: Den mest stabile forbindelse dannes af kovalent binding, hvor carbon deler sine 4 valenselektroner med fire fluoratomer. Dette resulterer i et stabilt molekyle, hvor hvert atom har en komplet oktet.
Andre faktorer:
* stabilitet: CF₄ er et meget stabilt molekyle på grund af de stærke kulstoffluorbindinger.
* fælles: Carbon tetrafluorid er en almindelig og velkendt forbindelse.
Sidste artikelHvad er den binære forbindelse til SO2?
Næste artikelHvad er det kovalente sammensatte navn på OS?
 Varme artikler
Varme artikler
-
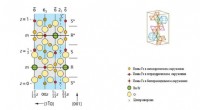 Forskere udvikler materialer til kvanteberegningKrystalstruktur af M-type hexagonal ferrit (en type magnetoplumbit). Kredit:South Ural State University (SUSU) Oprettelse af innovative materialer er et af de vigtigste områder af moderne videnska
Forskere udvikler materialer til kvanteberegningKrystalstruktur af M-type hexagonal ferrit (en type magnetoplumbit). Kredit:South Ural State University (SUSU) Oprettelse af innovative materialer er et af de vigtigste områder af moderne videnska -
 Et enkelt enzym inducerer det kemiske forsvar af en svamp mod larverKredit:Wiley Nogle svampe producerer langkædede umættede carboxylsyrer som deres kemiske forsvar mod insektlarver. Biosyntesen af disse polyener er kun afhængig af ét enzym, som tyske videnskabs
Et enkelt enzym inducerer det kemiske forsvar af en svamp mod larverKredit:Wiley Nogle svampe producerer langkædede umættede carboxylsyrer som deres kemiske forsvar mod insektlarver. Biosyntesen af disse polyener er kun afhængig af ét enzym, som tyske videnskabs -
 Oprettelse af mønstre spontant i syntetiske materialerEn polymerisationsfront markeret af varmegradienter (rød, højere temperatur) tillader spontan mønsterdannelse af polymerer med variable teksturer, farver og stivhed. Målestok, 1 cm. Kredit:Tilpasset f
Oprettelse af mønstre spontant i syntetiske materialerEn polymerisationsfront markeret af varmegradienter (rød, højere temperatur) tillader spontan mønsterdannelse af polymerer med variable teksturer, farver og stivhed. Målestok, 1 cm. Kredit:Tilpasset f -
 Teknik til at lave transparente polyethylenfilm så stærke som aluminiumKredit:CC0 Public Domain Forskning ledet af professor Ton Peijs fra WMG ved University of Warwick og professor Cees Bastiaansen ved Queen Mary University of London, har udtænkt en forarbejdningste
Teknik til at lave transparente polyethylenfilm så stærke som aluminiumKredit:CC0 Public Domain Forskning ledet af professor Ton Peijs fra WMG ved University of Warwick og professor Cees Bastiaansen ved Queen Mary University of London, har udtænkt en forarbejdningste


