Hvad er den afbalancerede ligning for ammoniumphosphat og natriumhydroxid?
(nh₄) ₃po₄ (aq) + 3 NaOH (aq) → 3 nh₃ (g) + na₃po₄ (aq) + 3 h₂o (l)
Her er en sammenbrud:
* reaktanter:
* Ammoniumphosphat ((NH₄) ₃po₄) er en opløselig ionisk forbindelse.
* Natriumhydroxid (NaOH) er også en opløselig ionisk forbindelse.
* Produkter:
* Ammoniak (NH₃) er en gas, der frigøres fra opløsningen.
* Natriumphosphat (Na₃po₄) er en opløselig ionisk forbindelse, der forbliver i opløsning.
* Vand (H₂O) dannes som en væske.
afbalancering af ligningen:
* Vi har brug for tre mol NaOH for at reagere med en mol (NH₄) ₃po₄ for at sikre, at antallet af hvert element på begge sider af ligningen er ens.
Denne reaktion er et eksempel på en dobbeltfortrængningsreaktion hvor de positive og negative ioner af reaktanterne skifter steder til dannelse af nye produkter.
Bemærk: Denne reaktion er også en syre-base-reaktion hvor ammoniumionen (NH₄⁺) fungerer som en syre, og hydroxidionen (OH⁻) fungerer som en base. Reaktionen resulterer i dannelsen af ammoniak (NH₃), en svag base og vand.
 Varme artikler
Varme artikler
-
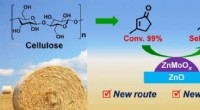 Forskere syntetiserer bio-baseret methylcyclopentadien med 3-methylcyclopent-2-enonDirekte hydrodeoxygenering af MCP til MCPD på den delvist reducerede Zn-Mo-oxidkatalysator. Kredit:DICP Methylcyclopentadien (MCPD) er en vigtig monomer i produktionen af RJ-4 brændstof, et rake
Forskere syntetiserer bio-baseret methylcyclopentadien med 3-methylcyclopent-2-enonDirekte hydrodeoxygenering af MCP til MCPD på den delvist reducerede Zn-Mo-oxidkatalysator. Kredit:DICP Methylcyclopentadien (MCPD) er en vigtig monomer i produktionen af RJ-4 brændstof, et rake -
 Ændring af silkeorms diæt til at spinde stærkere silkeSilkeormen og dens CNF-holdige foder. Kredit:Tohoku University Tohoku University forskere har produceret cellulose nanofiber (CNF) syntetiseret silke naturligt gennem en simpel tweak til silkeorms
Ændring af silkeorms diæt til at spinde stærkere silkeSilkeormen og dens CNF-holdige foder. Kredit:Tohoku University Tohoku University forskere har produceret cellulose nanofiber (CNF) syntetiseret silke naturligt gennem en simpel tweak til silkeorms -
 Nobelugen fortsætter med KemiprisenI denne mandag, 10. december, 2018 filbillede, en buste af Nobelprisstifteren, Alfred Nobel udstillet i Koncertsalen under Nobelprisuddelingen i Stockholm. Kontrovers forfølger Nobelpriserne for fred
Nobelugen fortsætter med KemiprisenI denne mandag, 10. december, 2018 filbillede, en buste af Nobelprisstifteren, Alfred Nobel udstillet i Koncertsalen under Nobelprisuddelingen i Stockholm. Kontrovers forfølger Nobelpriserne for fred -
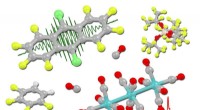 Kemikere udvikler nyt reagens til de-elektroneringPerhaloanthracen-radikalkationer delelektroniserer trimetaldodecacarbonyler under carbonmonoxidtryk for at danne de første klyngede overgangsmetalkationer. Kredit:Leveret af forskningsgruppen Kemik
Kemikere udvikler nyt reagens til de-elektroneringPerhaloanthracen-radikalkationer delelektroniserer trimetaldodecacarbonyler under carbonmonoxidtryk for at danne de første klyngede overgangsmetalkationer. Kredit:Leveret af forskningsgruppen Kemik
- Kan et eksemplar ses under mikroskop ved hjælp af 100x -målet uden dækglas?
- Hvordan beskriver du en del?
- Hvad er den kemiske formel for fluordas?
- Er skorpen og det øverste lag af mantel kaldet litosfære?
- Når havniveauet stiger, en stor del af Honolulu og Waikiki er sårbare over for oversvømmelse af g…
- Hvad er massen af en gennemsnitlig celle?


