Hvor mange gram natriumcarbonat indeholder 1,773 x 1017 carbonatomer?
1. Find molen af carbonatomer:
* Avogadros nummer fortæller os, at der er 6,022 x 10^23 atomer i en mol.
* Opdel antallet af carbonatomer med Avogadros nummer for at finde molen af kulstof:
(1.773 x 10^17 atomer) / (6.022 x 10^23 atomer / mol) =2,94 x 10^-7 mol C
2. Find molen af natriumcarbonat (NA2CO3):
* Formlen for natriumcarbonat viser, at der er et carbonatom pr. Molekyle natriumcarbonat.
* Da antallet af mol carbon og natriumcarbonat er ens i dette tilfælde, har vi 2,94 x 10^-7 mol Na2CO3.
3. Beregn massen af natriumcarbonat:
* Find den molære masse af natriumcarbonat:
* NA:22,99 g/mol (x2 =45,98 g/mol)
* C:12,01 g/mol
* O:16,00 g/mol (x3 =48,00 g/mol)
* Samlet molmasse:45,98 + 12,01 + 48,00 =105,99 g/mol
* Multiplicer molen af natriumcarbonat med dets molære masse:
(2,94 x 10^-7 mol) x (105,99 g/mol) = 3,12 x 10^-5 g Na2co3
Derfor indeholder 3,12 x 10^-5 gram natriumcarbonat 1,773 x 10^17 carbonatomer.
 Varme artikler
Varme artikler
-
 Fem mærkelige og vidunderlige måder naturen bliver udnyttet til at opbygge en bæredygtig modeindu…Enzymatiske tekstilfarvestoffer. Forfatter oplyst En af de største udfordringer for tekstil- og modeindustrien er at gøre sig selv mere bæredygtig, ikke kun hvad angår økonomiske og arbejdsmæssige
Fem mærkelige og vidunderlige måder naturen bliver udnyttet til at opbygge en bæredygtig modeindu…Enzymatiske tekstilfarvestoffer. Forfatter oplyst En af de største udfordringer for tekstil- og modeindustrien er at gøre sig selv mere bæredygtig, ikke kun hvad angår økonomiske og arbejdsmæssige -
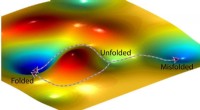 Skjult symmetri fundet i kemiske kinetiske ligningerEn kunstners repræsentation af et landskab med fri energi og to mulige veje, et protein kan følge (venstre) for at folde korrekt og en tredje vej (til højre), der fører til en fejlfoldet tilstand. Kre
Skjult symmetri fundet i kemiske kinetiske ligningerEn kunstners repræsentation af et landskab med fri energi og to mulige veje, et protein kan følge (venstre) for at folde korrekt og en tredje vej (til højre), der fører til en fejlfoldet tilstand. Kre -
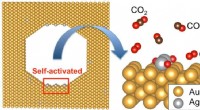 Håber på nye katalysatorer med høj aktivitetFigur:En aktiv struktur i en nanoporøs guldkatalysator. Kredit:Osaka University Guld er et metal, der er kemisk inaktivt og ikke korroderer, men nanoporøst guld (NPG), med dens svampelignende stru
Håber på nye katalysatorer med høj aktivitetFigur:En aktiv struktur i en nanoporøs guldkatalysator. Kredit:Osaka University Guld er et metal, der er kemisk inaktivt og ikke korroderer, men nanoporøst guld (NPG), med dens svampelignende stru -
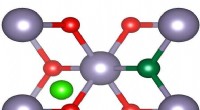 Discovery peger på vejen til bedre og billigere transparente ledereKompensation af acceptor fluorinterstitialer (lysegrøn) reducerer dramatisk elektronisk ydeevne af tindioxid gennemsigtige ledende glasbelægninger dopet med fluoratomer (mørkegrønne). Kredit:Universit
Discovery peger på vejen til bedre og billigere transparente ledereKompensation af acceptor fluorinterstitialer (lysegrøn) reducerer dramatisk elektronisk ydeevne af tindioxid gennemsigtige ledende glasbelægninger dopet med fluoratomer (mørkegrønne). Kredit:Universit
- Navngiv to objekter i solsystemet udover måner og planeter?
- Hvad er et sandkorn til stenblokke, som kører gennem rummet?
- Hvilken energi bruger du, når du trækker en vogn?
- Kød- og mejeriindustriens forsøg på at ændre måden, vi måler metan-emissioner på, ville slipp…
- Forskere finder sammenhæng mellem hurtigt smeltende arktisk is og havforsuring
- Hvem opdagede Einstein teorien om masse og energi?


