Hvad er formel for kobber I bisulfat?
Her er hvorfor:
* kobber (i) ioner (Cu+) er ustabile i vandige opløsninger. De er let uforholdsmæssige, hvilket betyder, at de reagerer med sig selv til dannelse af kobber (II) -ioner (Cu2+) og metallisk kobber (Cu):
2 Cu+ → Cu2++ Cu
* bisulfationer (HSO4-) er sure. De ville reagere med kobber (i) ioner og fremme yderligere uforholdsmæssig reaktion.
Derfor ville forsøg på at danne kobber (I) bisulfat sandsynligvis resultere i en blanding af kobber (II) sulfat, kobbermetal og svovlsyre.
 Varme artikler
Varme artikler
-
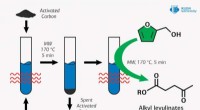 Chemist foreslår ny måde at forbedre brændstofkvaliteten ved hjælp af mikrobølgebestrålingKredit:RUDN Universitet En kemiker fra RUDN University har fundet en miljøvenlig måde at opnå estere af levulinsyre, der bruges som brændstoftilsætningsstof til kemisk syntese. Sammen med kolleger
Chemist foreslår ny måde at forbedre brændstofkvaliteten ved hjælp af mikrobølgebestrålingKredit:RUDN Universitet En kemiker fra RUDN University har fundet en miljøvenlig måde at opnå estere af levulinsyre, der bruges som brændstoftilsætningsstof til kemisk syntese. Sammen med kolleger -
 Forskere indser homogenisering af overfladeaktive steder af heterogen katalysatorKredit:Unsplash/CC0 Public Domain For nylig, et team ledet af professor Wu Changzheng fra School of Chemistry and Materials Science fra University of Science and Technology of China (USTC) i samar
Forskere indser homogenisering af overfladeaktive steder af heterogen katalysatorKredit:Unsplash/CC0 Public Domain For nylig, et team ledet af professor Wu Changzheng fra School of Chemistry and Materials Science fra University of Science and Technology of China (USTC) i samar -
 Ny undersøgelse finder unøjagtigheder i arseniske testsæt i BangladeshEfter en række trin med forskellige kemiske reagenser, farven, der udvikler sig på en teststrimmel, sammenlignes med et referenceskema leveret af sættets producent. En mørkere farve indikerer en højer
Ny undersøgelse finder unøjagtigheder i arseniske testsæt i BangladeshEfter en række trin med forskellige kemiske reagenser, farven, der udvikler sig på en teststrimmel, sammenlignes med et referenceskema leveret af sættets producent. En mørkere farve indikerer en højer -
 Ny metode til varmeledning kunne være en game changer for serverfarme og flyLaboratoriemedlem Mojtaba Edalatpour viser den termiske diode udviklet af Boreykos team. Kredit:Virginia Tech Jonathan Boreyko, en lektor i maskinteknik, har udviklet en termisk styringsteknologi
Ny metode til varmeledning kunne være en game changer for serverfarme og flyLaboratoriemedlem Mojtaba Edalatpour viser den termiske diode udviklet af Boreykos team. Kredit:Virginia Tech Jonathan Boreyko, en lektor i maskinteknik, har udviklet en termisk styringsteknologi
- Hvordan finder du, hvor mange atomer af et element, der er i en forbindelse, hvis kun får navnet og…
- Hvordan man nemt konverterer graders radianer (og grader)
- Hvis man observerer himlen fra den nordlige halvkugle, hvilken retning ville stjerner se ud til at b…
- Sådan konverteres pKa til Ka
- Hvor hurtigt er 53cc i MPH?
- Hvad er formålet med pollen, og hvor det producerede?


