Hvilken type reaktion sker, når kalium placeres i vand?
* reaktionstype: Enkelt forskydningsreaktion, også kendt som en redoxreaktion.
* Kemisk ligning: 2K (S) + 2H₂O (L) → 2KOH (AQ) + H₂ (G)
* Forklaring:
* Kalium (K) er et meget reaktivt alkalimetal.
* Det reagerer kraftigt med vand (H₂O) for at producere kaliumhydroxid (KOH), en stærk base og brintgas (H₂).
* Reaktionen frigiver en betydelig mængde varme, hvilket får brintgasen til at antænde og eksplodere.
* Den genererede varme kan få kalium til at smelte og endda antænde vandet.
Nøgleobservationer:
* fizzing: Hurtig dannelse af brintgasbobler.
* varme: Vandet opvarmes hurtigt og kan endda koge.
* flamme: Brintgassen antændes og skaber en lys flamme.
* røg: Små partikler af kaliumhydroxid kan frigøres som røg.
sikkerhed:
* Denne reaktion er ekstremt farlig og bør aldrig forsøges uden korrekt sikkerhedsudstyr og viden.
* Kalium skal altid håndteres med ekstrem forsigtighed og opbevares i et tørt, inert miljø.
* Bær altid passende sikkerhedsudstyr som handsker, beskyttelsesbriller og en laboratoriefrakke, når du håndterer kalium.
Fortæl mig, hvis du har andre spørgsmål.
 Varme artikler
Varme artikler
-
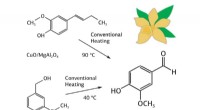 Kemiker skaber billige katalysatorer til produktion af vanillinKredit:RUDN University En kemiker fra RUDN University har skabt billige og effektive katalysatorer til produktion af vanillin ved hjælp af spinel -nanopartikler med kobberoxid -nanopartikler. Hydr
Kemiker skaber billige katalysatorer til produktion af vanillinKredit:RUDN University En kemiker fra RUDN University har skabt billige og effektive katalysatorer til produktion af vanillin ved hjælp af spinel -nanopartikler med kobberoxid -nanopartikler. Hydr -
 Billig tin pakker et stort slag for fremtiden for superkapacitorerForskere dopede koboltoxid med tin for at skabe en mere effektiv elektrode til brug i superkapacitorer. Dette mikroskopiske billede viser det nye materiale på grafenfilm. Kredit:JIa Zhu/Penn State
Billig tin pakker et stort slag for fremtiden for superkapacitorerForskere dopede koboltoxid med tin for at skabe en mere effektiv elektrode til brug i superkapacitorer. Dette mikroskopiske billede viser det nye materiale på grafenfilm. Kredit:JIa Zhu/Penn State -
 Verdens længste flaskebørstepolymer nogensinde syntetiseretFlaskebørstepolymer er en polymer bestående af en enkelt hovedkæde og adskillige sidekæder podet fra hovedkæden. Kredit:National Institute for Materials Science NIMS og RIKEN er lykkedes med at sy
Verdens længste flaskebørstepolymer nogensinde syntetiseretFlaskebørstepolymer er en polymer bestående af en enkelt hovedkæde og adskillige sidekæder podet fra hovedkæden. Kredit:National Institute for Materials Science NIMS og RIKEN er lykkedes med at sy -
 Løftet om dybe rillerDette viser siliciumskiver, i størrelse fra 4 ”til 12” diameter, som er blevet behandlet ved hjælp af Argonnes sekventielle infiltrationssyntesemetode. Kredit:Argonne National Laboratory En fremst
Løftet om dybe rillerDette viser siliciumskiver, i størrelse fra 4 ”til 12” diameter, som er blevet behandlet ved hjælp af Argonnes sekventielle infiltrationssyntesemetode. Kredit:Argonne National Laboratory En fremst
- Hvilket udsagn forklarer bedst, hvorfor en levende organisme i våd mount bevæger sig ind og ud af …
- Hvordan blomster bruger duft og nektar til at manipulere bestøvende planteædere
- Kan svovldioxid ændre lakmusfarven?
- Hvad sker der om natten under fotosynethese?
- Afdækning af det dominerende bidrag fra forbindelser med middel flygtighed til biomassebrændende o…
- Hvad er antropogen forstyrrelse?


