Natrium reagerer med ilt for at danne natriumoxid. Brug formlen nedenfor Bestem, hvor mange gram oxid der dannes, hvis der anvendes 46 som reaktion.?
1. Skriv den afbalancerede kemiske ligning:
4 na + o₂ → 2 na₂o
2. Bestem den molære masse af natrium (NA) og natriumoxid (Na₂o):
* NA:22,99 g/mol
* Na₂o:(22,99 g/mol * 2) + 16,00 g/mol =61,98 g/mol
3. Beregn molen af natrium:
* Mol na =masse af na / molær masse NA
* Mol Na =46 g / 22,99 g / mol =2 mol
4. Brug molforholdet fra den afbalancerede ligning:
* Den afbalancerede ligning viser, at 4 mol na reagerer på form 2 mol Na₂o.
5. Beregn molen af natriumoxid:
* Mol na₂o =(2 mol na) * (2 mol na₂o / 4 mol na) =1 mol na₂o
6. Beregn massen af natriumoxid:
* Masse na₂o =mol na₂o * molær masse na₂o
* Massen af Na₂o =1 mol * 61,98 g/mol =61,98 g
Svar: Hvis 46 gram natrium bruges i reaktionen, 61,98 gram af natriumoxid dannes.
Sidste artikelNår et mineral bryder langs svagt bundet fly?
Næste artikelHvad er de største ikke-varierende bestanddele af atmosfæren?
 Varme artikler
Varme artikler
-
 Spillets algoritme, der kan forbedre materialedesignKredit:Videnskab og teknologi af avancerede materialer Design af avancerede materialer er en kompleks proces, med mange potentielle kombinationer til præcist at placere atomer i en struktur. Men n
Spillets algoritme, der kan forbedre materialedesignKredit:Videnskab og teknologi af avancerede materialer Design af avancerede materialer er en kompleks proces, med mange potentielle kombinationer til præcist at placere atomer i en struktur. Men n -
 Forskere finder billigere, mindre energikrævende måde at rense ethylen påRasika Dias, UTA fremtrædende universitetsprofessor i kemi og biokemi Kredit:UTA Forskere ved University of Texas i Arlington har indgivet en foreløbig patentansøgning på en ny kobberforbindelse,
Forskere finder billigere, mindre energikrævende måde at rense ethylen påRasika Dias, UTA fremtrædende universitetsprofessor i kemi og biokemi Kredit:UTA Forskere ved University of Texas i Arlington har indgivet en foreløbig patentansøgning på en ny kobberforbindelse, -
 Forskere skal undersøge, om metalkorroderende mikrober kan vokse i Canadas foreslåede atomaffaldsa…Kredit:Pixabay/CC0 Public Domain Med Canada tættere på at flytte alt sit brugte nukleare brændsel til en enkelt facilitet og indkapsle hver brændstofbeholder i bentonit-ler, studerer forskere, om d
Forskere skal undersøge, om metalkorroderende mikrober kan vokse i Canadas foreslåede atomaffaldsa…Kredit:Pixabay/CC0 Public Domain Med Canada tættere på at flytte alt sit brugte nukleare brændsel til en enkelt facilitet og indkapsle hver brændstofbeholder i bentonit-ler, studerer forskere, om d -
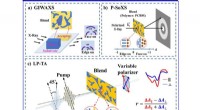 Undersøgelse af molekylær orientering ved polarisationsselektiv forbigående absorptionsspektrosko…Skematisk diagram over (a) GIWAXS, (b) P-SoXS og (c) LP-TA. Kredit:©Science China Press Den organiske solcelle (OSC) heterojunction -grænseflade er, hvor centrale fotofysiske processer som ladning
Undersøgelse af molekylær orientering ved polarisationsselektiv forbigående absorptionsspektrosko…Skematisk diagram over (a) GIWAXS, (b) P-SoXS og (c) LP-TA. Kredit:©Science China Press Den organiske solcelle (OSC) heterojunction -grænseflade er, hvor centrale fotofysiske processer som ladning
- Højopløsningsundersøgelse af Californiens kystklipperosion
- Carnegie Mellon og Near Earth Autonomy robotdroner stiller til show i Clemson
- Hvilket sukker er den mest almindelige energikilde?
- Navngivning af ny interstellar besøgende:2I/Borisov
- Hvad spreder havbunden som teorien om kontinentaldrift?
- Brug af dyb læring til at forudsige parametre for batterier på elektriske køretøjer


