Hvad er den procentvise koncentration af en 0,1N natriumhydoxidopløsning?
Forståelse af normalitet (n)
Normalitet er et mål for koncentration, der udtrykker antallet af gramækvivalenter af et opløst stof pr. Liter opløsning. For NaOH er et gramækvivalent lig med dens molære masse (40 g/mol).
Beregninger
1. Molaritet (M): Da 1 N NaOH -opløsning svarer til 1 M NaOH -opløsning, er en 0,1 N NaOH -opløsning også 0,1 M.
2. Mass af NaOH:
* 0,1 M NaOH betyder, at der er 0,1 mol NaOH pr. Liter opløsning.
* Masse NaOH =(0,1 mol/l) * (40 g/mol) =4 g/l
3. procentvis koncentration (w/v):
* Procentdelskoncentration (w/v) er massen af opløst stof (i gram) pr. 100 ml opløsning.
* Procentkoncentration (w/v) =(4 g/l) * (100 ml/l)/100 ml =0,4%
Derfor har en 0,1 N natriumhydroxidopløsning en procentvis koncentration på 0,4% (vægt/volumen).
 Varme artikler
Varme artikler
-
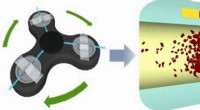 Fidget spinner som centrifuge adskiller blodplasmaKredit:American Chemical Society Nogle mennesker bruger fidget spinners - flade, legetøj med flere flige med et kugleleje i midten - for at sprede nervøs energi eller hvirvle stress væk. Nu, forsk
Fidget spinner som centrifuge adskiller blodplasmaKredit:American Chemical Society Nogle mennesker bruger fidget spinners - flade, legetøj med flere flige med et kugleleje i midten - for at sprede nervøs energi eller hvirvle stress væk. Nu, forsk -
 Nye materialer hjælper med at udvide volumetrisk 3-D-printVed hjælp af en tilpasset volumetrisk additiv fremstilling 3D-printer, Lawrence Livermore-forskere var i stand til at bygge hårde og stærke, samt strækbar og fleksibel, genstande næsten øjeblikkeligt
Nye materialer hjælper med at udvide volumetrisk 3-D-printVed hjælp af en tilpasset volumetrisk additiv fremstilling 3D-printer, Lawrence Livermore-forskere var i stand til at bygge hårde og stærke, samt strækbar og fleksibel, genstande næsten øjeblikkeligt -
 Forskere finder en ny måde at fremstille kemikalier på bæredygtigt ved at kopiere naturens tricksBakterier, der producerer kemikalier med (L) og uden (R) bioderivitiseringstrinnet. Med bioderivitisering, bakterierne er sundere (mørkere grønne). Kredit:Patrik Jones/Imperial College London Fors
Forskere finder en ny måde at fremstille kemikalier på bæredygtigt ved at kopiere naturens tricksBakterier, der producerer kemikalier med (L) og uden (R) bioderivitiseringstrinnet. Med bioderivitisering, bakterierne er sundere (mørkere grønne). Kredit:Patrik Jones/Imperial College London Fors -
 Bæredygtig nylonproduktion muliggjort ved opdagelse af bakterierArbejde med adipinsyrebakterier i Wallace Lab, University of Edinburgh. Kredit:The Wallace Lab, University of Edinburgh Nylonfremstilling kan revolutioneres ved opdagelsen af, at bakterier kan gør
Bæredygtig nylonproduktion muliggjort ved opdagelse af bakterierArbejde med adipinsyrebakterier i Wallace Lab, University of Edinburgh. Kredit:The Wallace Lab, University of Edinburgh Nylonfremstilling kan revolutioneres ved opdagelsen af, at bakterier kan gør


