Hvad er et direkte resultat af hydrogenbinding?
i kemi:
* Højere kogepunkter: Hydrogenbindinger mellem molekyler øger den energi, der kræves for at bryde dem fra hinanden, hvilket fører til højere kogepunkter for forbindelser som vand sammenlignet med lignende molekyler uden brintbinding.
* Øget viskositet: Hydrogenbinding gør væsker mere tyktflydende, når molekylerne holdes stærkere sammen.
* opløselighed: Hydrogenbinding bidrager til polære molekylers evne til at opløses i vand.
i biologi:
* Vands unikke egenskaber: Hydrogenbinding i vand gør det til et meget usædvanligt opløsningsmiddel med et højt kogepunkt, høj overfladespænding og evnen til at fungere som et universelt opløsningsmiddel for mange biologiske molekyler.
* Proteinstruktur: Hydrogenbindinger er kritiske for at opretholde den tredimensionelle struktur af proteiner og påvirke deres foldning og funktion.
* DNA -struktur: De to Strenge af DNA holdes sammen af brintbindinger mellem basisparene, som er afgørende for genetisk informationsopbevaring og replikation.
* Cellemembranstruktur: Hydrogenbinding hjælper med at stabilisere phospholipid -dobbeltlagsstrukturen af cellemembraner.
Andre vigtige resultater:
* krystaldannelse: Hydrogenbindinger bidrager til dannelsen af krystallinske strukturer i mange forbindelser.
* kapillær handling: Hydrogenbindinger bidrager til fænomenet kapillærvirkning, hvilket gør det muligt for vand at stige i smalle rør mod tyngdekraften.
I sidste ende er de direkte resultater af hydrogenbinding forskellige og vidtrækkende, hvilket påvirker stoffets fysiske og kemiske egenskaber og spiller en kritisk rolle i mange biologiske processer.
Sidste artikelHvad er middel mod forurening?
Næste artikelElement i Halide -familien, der er flydende?
 Varme artikler
Varme artikler
-
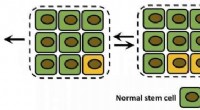 Kemikers beregninger kan fremme forudsigelse af kræftEn skematisk viser en enkelt mutationsfikseringsproces i et vævsrum. Normale stamceller er grønne, og muterede celler er gule. Rice University-forskere brugte en diskret statistisk stokastisk model ti
Kemikers beregninger kan fremme forudsigelse af kræftEn skematisk viser en enkelt mutationsfikseringsproces i et vævsrum. Normale stamceller er grønne, og muterede celler er gule. Rice University-forskere brugte en diskret statistisk stokastisk model ti -
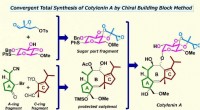 Total syntese af cotylenin A til et nyt kræftlægemiddel uden bivirkningerKredit:Nakada Laboratory, Waseda Universitet Det lykkedes for forskere ved Waseda University at udvikle en metode til en total syntese af cotylenin A, en plantevækstregulator, som har tiltrukket s
Total syntese af cotylenin A til et nyt kræftlægemiddel uden bivirkningerKredit:Nakada Laboratory, Waseda Universitet Det lykkedes for forskere ved Waseda University at udvikle en metode til en total syntese af cotylenin A, en plantevækstregulator, som har tiltrukket s -
 Udskrivbar, farverig camouflage med polymererNyudviklet polymer kan bedre efterligne naturens farveskiftende evner. Kredit:American Chemical Society I naturen, farver kan fungere som en form for kommunikation, men de kan også skjule dyr og p
Udskrivbar, farverig camouflage med polymererNyudviklet polymer kan bedre efterligne naturens farveskiftende evner. Kredit:American Chemical Society I naturen, farver kan fungere som en form for kommunikation, men de kan også skjule dyr og p -
 Design af næste generation af hårfarverTova Williams, en ph.d. studerende ved North Carolina State University, laver forskning, der er relevant for de 75 procent af amerikanske kvinder, der farver deres hår, og de stylister, der anvender d
Design af næste generation af hårfarverTova Williams, en ph.d. studerende ved North Carolina State University, laver forskning, der er relevant for de 75 procent af amerikanske kvinder, der farver deres hår, og de stylister, der anvender d
- Hvor mange hydroxidioner er nødvendige for at danne en neutral ionisk forbindelse med en aluminiumi…
- Når tilsætning af varme, hvad ændrer det en væske til?
- Ny Boeing CEO er en veteran fra virksomheden, som vil blive testet
- Organisationer med brede sociale bånd hjælper med at komme sig efter naturkatastrofer
- Hvad blev brugt til opvarmning og lys før elektrisk energi?
- Hvad er forskellene mellem en indfaldende stråle og en reflektionsstråle?


