Hvad er molariteten af et sølvnitrat, der indeholder 42,5 g AGNO3 i 100 ml opløsning?
1. Find den molære masse af Agno3:
* AG (sølv):107,87 g/mol
* N (nitrogen):14,01 g/mol
* O (ilt):16,00 g/mol (x 3 =48,00 g/mol)
* Samlet molmasse af Agno3 =107,87 + 14,01 + 48,00 =169,88 g/mol
2. Konverter massen af Agno3 til mol:
* Mol AgnO3 =(42,5 g) / (169,88 g / mol) =0,250 mol
3. Konverter mængden af løsningen til liter:
* 100 ml =0,100 l
4. Beregn molariteten (M):
* Molaritet (m) =(mol opløst stof) / (liter opløsning)
* M =(0,250 mol) / (0,100 l) =2,50 m
Derfor er molariteten af sølvnitratopløsningen 2,50 m.
 Varme artikler
Varme artikler
-
 Kemikere ændrer bindingerne mellem atomer i et enkelt molekyle for første gangBilleder af enkelte molekyler opnået ved højopløsnings atomkraftmikroskopi. Selektivt og reversibelt kan den molekylære struktur i midten omdannes til strukturen til højre eller venstre, ved at spændi
Kemikere ændrer bindingerne mellem atomer i et enkelt molekyle for første gangBilleder af enkelte molekyler opnået ved højopløsnings atomkraftmikroskopi. Selektivt og reversibelt kan den molekylære struktur i midten omdannes til strukturen til højre eller venstre, ved at spændi -
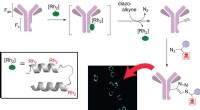 Metal forenkler syntesen af antistoflægemidlerRice University-kemikere har designet et plug-in metalloprotein for at forenkle opgaven med at lave målrettede antistofterapier. Forskerne brugte et tredobbeltmetaliseret peptid (indsat) til at give e
Metal forenkler syntesen af antistoflægemidlerRice University-kemikere har designet et plug-in metalloprotein for at forenkle opgaven med at lave målrettede antistofterapier. Forskerne brugte et tredobbeltmetaliseret peptid (indsat) til at give e -
 Nyt elektrodemateriale udviklet til at øge opladningskapaciteten af lithium-batterierNyt elektrodemateriale udviklet til at øge opladningskapaciteten af lithium-batterier. Kredit:Yokohama National University Lithium-batterier lover meget for fremtiden for mange applikationer, he
Nyt elektrodemateriale udviklet til at øge opladningskapaciteten af lithium-batterierNyt elektrodemateriale udviklet til at øge opladningskapaciteten af lithium-batterier. Kredit:Yokohama National University Lithium-batterier lover meget for fremtiden for mange applikationer, he -
 Nyt materiale udsender hvidt lys, når det udsættes for elektricitetElektrisk-stimuli-responsive porøse kulstof-nanoreringer med jod. En elektrisk stimulus inducerer kulbrinte-nanoring cycloparaphenylen (CPP)-iod-samlingen til at vise elektronisk ledningsevne og hvidt
Nyt materiale udsender hvidt lys, når det udsættes for elektricitetElektrisk-stimuli-responsive porøse kulstof-nanoreringer med jod. En elektrisk stimulus inducerer kulbrinte-nanoring cycloparaphenylen (CPP)-iod-samlingen til at vise elektronisk ledningsevne og hvidt
- Hvor mange elektroner låner brom?
- Hvilket giver et mere nøjagtigt billede af jorden - kort eller kloden forklare?
- Hurtig 3D-print med synligt lys
- En videnskabsmand, der forsøger at bestemme, hvorfor dryss salt på en iskald vej får isen til at …
- Hvad sker der, når lys passerer gennem et plasma?
- Nyt håndtag til styring af elektromagnetiske egenskaber kunne muliggøre spintronisk databehandling


