Hvad er reaktionsligningen for ammoniumchlorid og vand?
Her er den afbalancerede kemiske ligning:
nh₄cl (aq) + h₂o (l) ⇌ nh₃ (aq) + h₃o⁺ (aq) + cl⁻ (aq)
Forklaring:
* nh₄cl (aq) Repræsenterer ammoniumchlorid opløst i vand.
* h₂o (l) repræsenterer flydende vand.
* nh₃ (aq) Repræsenterer ammoniak opløst i vand.
* h₃o⁺ (aq) Repræsenterer hydroniumioner opløst i vand.
* cl⁻ (aq) Repræsenterer chloridioner opløst i vand.
Vigtig note: Reaktionen er reversibel (indikeret af dobbeltpilene ⇌), hvilket betyder, at ammoniak- og hydroniumioner også kan reagere på dannelse af ammoniumioner og vand. Dette er grunden til, at opløsningen vil indeholde en blanding af alle disse ioner i ligevægt.
Reaktionen er let sur Fordi hydroniumionerne produceret ved hydrolyse af ammoniumchlorid gør opløsningen mere sur end rent vand.
 Varme artikler
Varme artikler
-
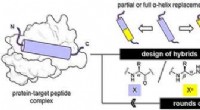 Oligourea foldamerer efterligner peptider alfa-helices og binder effektivt til lægemiddelmålKredit:Wiley Nogle nyttige lægemidler består af peptider, der virker på deres proteinmål. For at gøre dem mere effektive og stabile, forskere har fundet en måde at erstatte afgørende segmenter af
Oligourea foldamerer efterligner peptider alfa-helices og binder effektivt til lægemiddelmålKredit:Wiley Nogle nyttige lægemidler består af peptider, der virker på deres proteinmål. For at gøre dem mere effektive og stabile, forskere har fundet en måde at erstatte afgørende segmenter af -
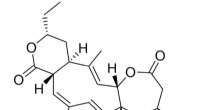 Et usædvanligt molekyle beskytter nerveceller mod degenerationDen kemiske struktur af collinolacton. Kredit:University of Tübingen Et internationalt forskerhold ledet af professor Stephanie Grond fra Institute of Organic Chemistry ved University of Tübingen
Et usædvanligt molekyle beskytter nerveceller mod degenerationDen kemiske struktur af collinolacton. Kredit:University of Tübingen Et internationalt forskerhold ledet af professor Stephanie Grond fra Institute of Organic Chemistry ved University of Tübingen -
 Ny metode til at fjerne olie fra vandEn dråbe råolie på en vandoverflade adsorberes inden for få sekunder af et blad af den flydende bregne Salvinia og trækkes op af vandet. Kredit:W. Barthlott, M. Mail/Uni Bonn Olie udgør en betydel
Ny metode til at fjerne olie fra vandEn dråbe råolie på en vandoverflade adsorberes inden for få sekunder af et blad af den flydende bregne Salvinia og trækkes op af vandet. Kredit:W. Barthlott, M. Mail/Uni Bonn Olie udgør en betydel -
 Ny metode til fremstilling af prækursorer til højstyrke kulfiberforarbejdningDet kan bruges til at producere kulfiber med nye forbedrede egenskaber. Kredit:Lobachevsky University Kulfiber er et vigtigt strukturelt materiale. På grund af sin høje styrke, i kombination med l
Ny metode til fremstilling af prækursorer til højstyrke kulfiberforarbejdningDet kan bruges til at producere kulfiber med nye forbedrede egenskaber. Kredit:Lobachevsky University Kulfiber er et vigtigt strukturelt materiale. På grund af sin høje styrke, i kombination med l
- Hvad kaldte du en strøm, der bevæger sig i ledning?
- Hvor meget koster delen?
- Hvilke elektromagnetiske bølger produceres af stjerner og galakser?
- Fysikere udarbejder metode til at afsløre, hvordan lys påvirker materialer
- Aggressionsde-eskaleringsgen identificeret i frugtfluer
- Leica genopliver det ikoniske sovjetiske Zenit-kamera


