Hvad er molariteten af en 0,142 M Na3 PO4 -opløsning, der har densitet 1,015 g m l viser alle trin?
Her er hvorfor:
* Molaritet (M): Repræsenterer koncentrationen af en opløsning. Det fortæller dig, hvor mange mol af et stof (opløst stof) opløses i et specifikt volumen (normalt liter) af opløsningen.
* densitet: Er et mål på masse pr. Enhedsvolumen. I dette tilfælde fortæller det dig, hvor meget masse af opløsningen der er pakket i hver milliliter.
Den givne densitetsinformation (1.015 g/ml) påvirker ikke molariteten af opløsningen. Opløsningen er allerede angivet at være 0,142 m na₃po₄.
Forklaring:
Forestil dig, at du har en 1-liters løsning på 0,142 m na₃po₄. Denne opløsning indeholder 0,142 mol na₃po₄. Uanset om opløsningen er tæt eller mindre tæt, forbliver mængden af na₃po₄, der er til stede i denne liter, den samme, så molariteten forbliver konstant.
Vigtig note: Hvis du ville beregne * messen * af na₃po₄ til stede i et bestemt volumen af løsningen, ville densiteten være vigtig.
Sidste artikelHvad er forbindelser, der indeholder kulstof som det primære strukturelle atom?
Næste artikelHvad hedder Compound VO3?
 Varme artikler
Varme artikler
-
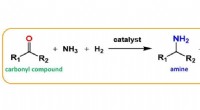 For meget aktive, bæredygtige katalysatorer, bare tilsæt fosforFig. 1. Reduktiv amination af carbonylforbindelser. Kredit:Osaka University Katalysatorer er afgørende for at gøre industrielle processer levedygtige. Imidlertid, mange af de ikke-ædelmetalkatalys
For meget aktive, bæredygtige katalysatorer, bare tilsæt fosforFig. 1. Reduktiv amination af carbonylforbindelser. Kredit:Osaka University Katalysatorer er afgørende for at gøre industrielle processer levedygtige. Imidlertid, mange af de ikke-ædelmetalkatalys -
 Opsamling af rent vand fra luften, inspireret af ørkenlivetKredit:CC0 Public Domain Mennesker kan klare sig i de mest basale krisecentre, kan ridse et måltid sammen af de mest ydmyge ingredienser. Men vi kan ikke overleve uden rent vand. Og på steder, h
Opsamling af rent vand fra luften, inspireret af ørkenlivetKredit:CC0 Public Domain Mennesker kan klare sig i de mest basale krisecentre, kan ridse et måltid sammen af de mest ydmyge ingredienser. Men vi kan ikke overleve uden rent vand. Og på steder, h -
 Forskere udvikler billige, høj strømtæthed vanadium flow batteri stakNy generation af vanadiumflow-batteristabelteknologi tilbyder lave omkostninger og høj effekttæthed. Kredit:SHI Dingqin Udviklingen af vedvarende energikilder såsom vind- og solenergi er begræns
Forskere udvikler billige, høj strømtæthed vanadium flow batteri stakNy generation af vanadiumflow-batteristabelteknologi tilbyder lave omkostninger og høj effekttæthed. Kredit:SHI Dingqin Udviklingen af vedvarende energikilder såsom vind- og solenergi er begræns -
 Nyt materiale gør køleudstyr mere energieffektiveTil deres prøver, de dækkede en konventionel varmeveksler (som brugt i kommercielt køleudstyr) med det nye materiale, i samarbejde med kolleger fra Fraunhofer Institute for Solar Energy Systems. Kredi
Nyt materiale gør køleudstyr mere energieffektiveTil deres prøver, de dækkede en konventionel varmeveksler (som brugt i kommercielt køleudstyr) med det nye materiale, i samarbejde med kolleger fra Fraunhofer Institute for Solar Energy Systems. Kredi
- Hvad er eksempler på alternative former energi?
- Hvordan påvirker kraft tilstanden for bevægelsesobjekter?
- Forskere påviser transport af mekanisk energi, selv gennem beskadigede veje
- Rumskib 1 og 2 har lige store masser på 300 kg har en indledende momentumstørrelse 600 ms Hvad er …
- hvirvlet til venstre eller højre? Nanofibre justeres i omrørt væske
- Fingeraftryksspektroskopi inden for et millisekund


