Hvad sker der med de individuelle atomer i en kemisk reaktion?
* atomer oprettes ikke eller ødelægges: Dette er det grundlæggende princip i loven om bevarelse af masse. I en kemisk reaktion er atomerne, der er til stede i starten, stadig til stede i slutningen, bare omarrangeret.
* atomer omarrangeres: Kemiske reaktioner involverer brud og dannelse af kemiske bindinger mellem atomer. Atomerne forbliver intakte, men ændrer deres partnerskaber for at danne nye molekyler.
* obligationer er brudt og dannet: Den energi, der kræves for at bryde eksisterende obligationer, kommer fra det omgivende miljø, og dannelsen af nye obligationer frigiver energi.
* nye stoffer dannes: Omarrangering af atomer i nye kombinationer skaber nye stoffer med forskellige egenskaber end de originale reaktanter.
Analogi:
Forestil dig at opbygge en LEGO -struktur. Du har et sæt individuelle LEGO -mursten (atomer), som du omarrangerer for at oprette forskellige modeller (molekyler). Du kan bryde eksisterende modeller fra hinanden og genopbygge dem til nye, men du har altid det samme antal mursten (atomer) i begyndelsen og slutningen.
Eksempel:
Forbrændingen af methan (CH4) med ilt (O2) producerer kuldioxid (CO2) og vand (H2O).
* reaktanter: CH4 + 2 O2
* Produkter: CO2 + 2 H2O
De kulstof-, brint- og iltatomer, der er til stede i metan- og iltmolekylerne, omarrangeres til dannelse af kuldioxid og vandmolekyler. Det samlede antal af hver type atom forbliver det samme.
 Varme artikler
Varme artikler
-
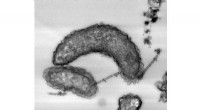 Jernætsende bakterier har vist sig at have enzymer, der gør dem i stand til at udvinde elektroner …Figur:Transmissionselektronmikroskopisk billede af ydre membrancytokromer under elektronkildemangel. Ydre membran (OM) Cytokromer blev farvet på celleoverfladen og nanotråde. Kredit:National Institute
Jernætsende bakterier har vist sig at have enzymer, der gør dem i stand til at udvinde elektroner …Figur:Transmissionselektronmikroskopisk billede af ydre membrancytokromer under elektronkildemangel. Ydre membran (OM) Cytokromer blev farvet på celleoverfladen og nanotråde. Kredit:National Institute -
 Bygge vægge, der vil gøre sommerens hedebølger mere tålelige(a) PCM-vægtværsnit (b) temperaturmålingsposition. Kredit:Korea Institute of Science and Technology (KIST) Med sommervarmen, der bliver mere og mere uudholdelig og langvarig på grund af klimaændri
Bygge vægge, der vil gøre sommerens hedebølger mere tålelige(a) PCM-vægtværsnit (b) temperaturmålingsposition. Kredit:Korea Institute of Science and Technology (KIST) Med sommervarmen, der bliver mere og mere uudholdelig og langvarig på grund af klimaændri -
 Video:Coronavirus-vaccine:Hvor er vi, og hvad er det næste?Kredit:The American Chemical Society Du har måske hørt, at COVID-19-vaccineforsøg er i gang i Seattle. Hvad er det præcist, der testes? Hvor meget længere vil disse test tage? Og hvornår kan vi f
Video:Coronavirus-vaccine:Hvor er vi, og hvad er det næste?Kredit:The American Chemical Society Du har måske hørt, at COVID-19-vaccineforsøg er i gang i Seattle. Hvad er det præcist, der testes? Hvor meget længere vil disse test tage? Og hvornår kan vi f -
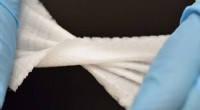 3D-trykt Biomesh minimerer brokreparationskomplikationer3D -printet Biomesh demonstrerer sin mekaniske styrke og fleksibilitet. Kredit:Baylor College of Medicine Brok er en af de mest almindelige bløde vævsskader. Brok dannes ved intra-abdominal indh
3D-trykt Biomesh minimerer brokreparationskomplikationer3D -printet Biomesh demonstrerer sin mekaniske styrke og fleksibilitet. Kredit:Baylor College of Medicine Brok er en af de mest almindelige bløde vævsskader. Brok dannes ved intra-abdominal indh
- Kan du se Planet Mercury om natten?
- Forbedring af menneske-data-interaktion for at fremskynde innovation af nanomaterialer
- Hvor mange atomer er der i oxygengas?
- Hvad gør tyngdekraften mellem to objekter?
- Hvorfor bliver skyer mørke, når det er ved at storme?
- Hvad er de seks mest almindelige elementer i levende organismer?


