Hvilket atom mister sit elektron let, er det carbon kaliumlithium eller brint?
* ioniseringsenergi: Ioniseringsenergi er den mængde energi, der kræves for at fjerne et elektron fra et atom. Atomer med lavere ioniseringsenergier mister elektroner lettere.
* atomstruktur:
* lithium: Lithium har kun et elektron i sin yderste skal. Denne elektron er relativt langt fra kernen og oplever svagere tiltrækning, hvilket gør det lettere at fjerne.
* kalium: Kalium har også et enkelt elektron i sin yderste skal, men det er længere nede på det periodiske bord, hvilket gør det endnu mere reaktivt end lithium.
* brint: Hydrogen har kun en elektron, men det er meget tæt bundet til dens kerne.
* carbon: Carbon har fire valenselektroner, og det ønsker generelt at dele elektroner i stedet for at miste dem.
Kortfattet: Lithium har den laveste ioniseringsenergi blandt de anførte indstillinger, hvilket gør det til atomet, der mister sin elektron let.
Sidste artikelHvad er blyoxid og kulstof lige?
Næste artikelHvilke gasser er elementer?
 Varme artikler
Varme artikler
-
 En bioplast, der beskytter mod UV-strålingKredit:Oulu Universitet Forskere ved Uleåborgs universitets forskningsenhed for bæredygtig kemi har udviklet en ny syntetisk bioplast, der i modsætning til traditionel kulstofbaseret plast eller a
En bioplast, der beskytter mod UV-strålingKredit:Oulu Universitet Forskere ved Uleåborgs universitets forskningsenhed for bæredygtig kemi har udviklet en ny syntetisk bioplast, der i modsætning til traditionel kulstofbaseret plast eller a -
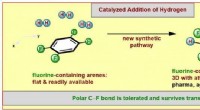 En ny metode til dannelse af fluorerede molekylære ringeillustration af den nye syntetiske metode. Kredit:WWU/Frank Glorius Farvestoffer, lægemidler, og funktionelle materialer er generelt baseret på innovative molekyler fremstillet af kemikere. Til de
En ny metode til dannelse af fluorerede molekylære ringeillustration af den nye syntetiske metode. Kredit:WWU/Frank Glorius Farvestoffer, lægemidler, og funktionelle materialer er generelt baseret på innovative molekyler fremstillet af kemikere. Til de -
 Forskere identificerer et molekyle, der kunne have hjulpet celler med at overleve - og trives - på …Protoceller ville have været forfædre til celler i dag, hvis du vil, ” siger Ramanarayanan Krishnamurthy, PhD, en lektor i kemi ved Scripps Research. De havde ikke den fulde funktionalitet af moderne
Forskere identificerer et molekyle, der kunne have hjulpet celler med at overleve - og trives - på …Protoceller ville have været forfædre til celler i dag, hvis du vil, ” siger Ramanarayanan Krishnamurthy, PhD, en lektor i kemi ved Scripps Research. De havde ikke den fulde funktionalitet af moderne -
 Brug af neutroner til at studere, hvordan resistente bakterier udvikler sigBakterier, der indeholder enzymer kaldet beta-lactamaser, illustreret af den lyseblå klynge, nedbryde antibiotika og tillader bakterielle infektioner at udvikle sig og spredes gennem menneskelige cell
Brug af neutroner til at studere, hvordan resistente bakterier udvikler sigBakterier, der indeholder enzymer kaldet beta-lactamaser, illustreret af den lyseblå klynge, nedbryde antibiotika og tillader bakterielle infektioner at udvikle sig og spredes gennem menneskelige cell
- Biobaseret gødning som løsning til fosfortilstrækkelighed og reducerede drivhusgasemissioner
- Er det rigtigt, at massen ændrer sig, når tyngdekraften ændrer sig?
- Barndom i middelalderens Bayern:Hvad tænder afslører om ernæring og migration
- Hvad er kogepunktet for monster energi?
- Stratusskyer kan være forbundet med hvilken slags front?
- Se verdens højeste glasbro få slædehamret


