Hvad sker der, hvis du blander jernsulfat og natriumhydroxid?
Her er den afbalancerede kemiske ligning for reaktionen:
fe₂ (so₄) ₃ (aq) + 6naOH (aq) → 2Fe (OH) ₃ (s) + 3na₂so₄ (aq)
Forklaring:
* jernsulfat (Fe₂ (SO₄) ₃) er en opløselig ionisk forbindelse, der adskiller sig i fe³⁺ -ioner og so₄²⁻ ioner i vand.
* natriumhydroxid (NaOH) er også en opløselig ionisk forbindelse, der dissocieres i Na⁺ -ioner og OH⁻ioner i vand.
* Når disse opløsninger er blandet, reagerer Fe³⁺ -ioner fra jernsulfat med OH⁻ -ioner fra natriumhydroxid til dannelse af jernhydroxid (Fe (OH) ₃) .
* Ferrisk hydroxid er en uopløselig forbindelse og udfælder derfor ud af opløsningen som et rødbrunt fast stof.
* De resterende ioner, Na⁺ og So₄²⁻, forbliver i opløsningen som natriumsulfat (na₂so₄) .
Observationer:
* Du vil observere dannelsen af et rødbrunt bundfald (jernhydroxid) i opløsningen.
* Løsningen kan blive lidt overskyet eller uigennemsigtig på grund af bundfaldet.
* Reaktionen er eksoterm, hvilket betyder, at den frigiver varme, og opløsningen kan føles lidt varmere.
Vigtig note:
Denne reaktion er et eksempel på en dobbeltfortrængningsreaktion hvor kationerne og anionerne af reaktanterne skifter partnere for at danne nye produkter. Dannelsen af den uopløselige jernhydroxid driver reaktionen fremad.
Sidste artikelHvad er det samlede antal valenselektroner i en atomnitrogen jordtilstand?
Næste artikelHvad mineral giver af partikler?
 Varme artikler
Varme artikler
-
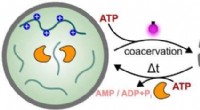 Hvordan lys kan bruges til at styre processer i syntetiske cellerKredit:Shoupeng Cao et al., Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202205266 Syntetiske (kunstigt producerede) celler kan efterligne visse funktioner af biologiske celler.
Hvordan lys kan bruges til at styre processer i syntetiske cellerKredit:Shoupeng Cao et al., Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202205266 Syntetiske (kunstigt producerede) celler kan efterligne visse funktioner af biologiske celler. -
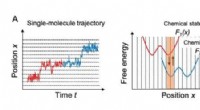 Matematisk modellering afslører, hvordan chitinase, en molekylær monorail, adlyder et envejsskiltFig. 1. (A) Bane for enkeltmolekylær bevægelse og tilsvarende kemisk-tilstandsafhængige frie energiprofiler. (B) Skematisk af en skjult Markov -model, hvor de kemiske tilstande betragtes som skjulte t
Matematisk modellering afslører, hvordan chitinase, en molekylær monorail, adlyder et envejsskiltFig. 1. (A) Bane for enkeltmolekylær bevægelse og tilsvarende kemisk-tilstandsafhængige frie energiprofiler. (B) Skematisk af en skjult Markov -model, hvor de kemiske tilstande betragtes som skjulte t -
 Undersøgelse ser til is for at fremstille nyttige porøse materialerXiao Cheng Zeng (til venstre) og Chonqin Zhou. Kredit:University of Nebraska-Lincoln At opdage en måde at udnytte isrekrystallisering på kunne muliggøre fremstilling af højeffektive materialer til
Undersøgelse ser til is for at fremstille nyttige porøse materialerXiao Cheng Zeng (til venstre) og Chonqin Zhou. Kredit:University of Nebraska-Lincoln At opdage en måde at udnytte isrekrystallisering på kunne muliggøre fremstilling af højeffektive materialer til -
 Holdbare træsvampe fungerer som grønne sensorer for mekanisk belastningPå dette fotografi, en træ carbon svamp genopretter til sin oprindelige form efter komprimering. Kredit:Chen et al. Slå den helt rigtige balance mellem blødhed og robusthed, balsatræ er et valgmat
Holdbare træsvampe fungerer som grønne sensorer for mekanisk belastningPå dette fotografi, en træ carbon svamp genopretter til sin oprindelige form efter komprimering. Kredit:Chen et al. Slå den helt rigtige balance mellem blødhed og robusthed, balsatræ er et valgmat
- Hvilken er overførslen af varme gennem et materiale uden bevægelse i sig selv?
- Elektronopførende nanopartikler skubber den nuværende forståelse af stof
- Fransk opfinder svæver over den engelske kanal på flyboard
- ALMA finder massive urgalakser, der svømmer i et stort hav af mørkt stof
- Hvad gør acet coenzym a?
- Hvordan kan du føle en styrke på 1N?


