Du skabte phosphatbuffer hvid pH 8,5 og opbevares derefter i køleskab bliver krystallin hvorfor?
opløselighed og temperatur:
* fosfatsalte er mindre opløselige ved lavere temperaturer. Når du opbevarer din buffer i køleskabet, får den koldere temperatur opløseligheden af fosfatsalteene til at falde.
* Krystallisation: Når opløseligheden falder, kan fosfationerne ikke længere forblive fuldt opløst i opløsningen. De begynder at komme ud af opløsningen og danne krystaller.
Andre faktorer:
* Bufferkoncentration: Mere koncentrerede phosphatbuffere er mere tilbøjelige til krystallisation, fordi der er en højere koncentration af fosfationer, der kan komme ud af opløsningen.
* specifikke salte: Forskellige fosfatsalte har forskellige opløseligheder. For eksempel er dibasisk natriumphosphat (Na2HPO4) generelt mere opløselig end monobasisk natriumphosphat (NAH2PO4).
* ph: PH af bufferen kan også påvirke opløselighed.
hvordan man forhindrer krystallisation:
* lavere koncentration: Brug en lavere koncentration af phosphatsalte, hvis det er muligt.
* Varm op før brug: Før du bruger pufferen, skal du varme den til stuetemperatur for at øge opløseligheden af fosfatsalte.
* Brug et andet buffersystem: Hvis du har brug for en buffer ved pH 8,5, der er mindre tilbøjelig til krystallisation, skal du overveje at bruge et andet buffersystem som Tris eller HEPES.
Vigtig note: Hvis du ser krystaller i din buffer, er det bedst at kassere den. Mens bufferen stadig kan være funktionel efter opløsning af krystallerne, kan deres tilstedeværelse indikere et potentielt problem med pufferens stabilitet.
Sidste artikelEr butyl en leder eller isolator?
Næste artikelAfbalanceret symbolligning for kaliumhydroxid?
 Varme artikler
Varme artikler
-
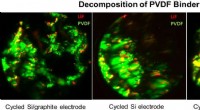 Mod omkostningseffektive løsninger til næste generations forbrugerelektronik, elbiler og elnetNedbrydningen af et polyvinylidenfluorid (PVDF) bindemiddel i et højenergibatteri. Kredit:Jigang Zhou Jagten på et bedre lithium-ion-batteri - et, der kunne holde en mobiltelefon i gang i dagevi
Mod omkostningseffektive løsninger til næste generations forbrugerelektronik, elbiler og elnetNedbrydningen af et polyvinylidenfluorid (PVDF) bindemiddel i et højenergibatteri. Kredit:Jigang Zhou Jagten på et bedre lithium-ion-batteri - et, der kunne holde en mobiltelefon i gang i dagevi -
 Livets kilde:Vanddråber rummer den hemmelige ingrediens til at opbygge livKredit:CC0 Public Domain Purdue University kemikere har afsløret en mekanisme til, at peptiddannende reaktioner kan forekomme i vand - noget, der har undret videnskabsmænd i årtier. Dette er i bun
Livets kilde:Vanddråber rummer den hemmelige ingrediens til at opbygge livKredit:CC0 Public Domain Purdue University kemikere har afsløret en mekanisme til, at peptiddannende reaktioner kan forekomme i vand - noget, der har undret videnskabsmænd i årtier. Dette er i bun -
 Video:Hvordan måler vi temperatur?Kredit:The American Chemical Society Vi har stor tillid til, at vi måler temperaturen nøjagtigt. Men hvordan fungerer termometre i køkkenet eller på lægekontoret? Takket være termodynamikkens love
Video:Hvordan måler vi temperatur?Kredit:The American Chemical Society Vi har stor tillid til, at vi måler temperaturen nøjagtigt. Men hvordan fungerer termometre i køkkenet eller på lægekontoret? Takket være termodynamikkens love -
 Forskere renser dramatisk op i ammoniakproduktionen og reducerer omkostningerneSWAP-processen i aktion. Den omdanner effektivt 90 procent af råmaterialet til ammoniak på én gang, hvorimod Haber-Bosch-processen kun konverterer 10 pct. Kredit:2019 Yoshiaki Nishibayashi Ammonia
Forskere renser dramatisk op i ammoniakproduktionen og reducerer omkostningerneSWAP-processen i aktion. Den omdanner effektivt 90 procent af råmaterialet til ammoniak på én gang, hvorimod Haber-Bosch-processen kun konverterer 10 pct. Kredit:2019 Yoshiaki Nishibayashi Ammonia


