Hvad vil øge gasvolumenet?
* stigende temperatur: Når du opvarmer en gas, bevæger partiklerne sig hurtigere og kolliderer hyppigere med væggene i deres beholder. Dette øgede tryk resulterer i et større volumen.
* faldende pres: Hvis du reducerer presset på en gas, har partiklerne mere plads til at bevæge sig rundt i. Dette resulterer i en stigning i volumen.
* Tilføjelse af mere gas: Forøgelse af antallet af gasmolekyler (mol) i en beholder vil også øge volumenet, forudsat at temperaturen og trykket forbliver konstant.
Vigtig note: Disse forhold er baseret på den ideelle gaslov, der antager ideelle forhold (ingen intermolekylære kræfter, perfekt elastiske kollisioner osv.). I scenarier i den virkelige verden kan disse forhold være let modificerede.
Sidste artikelHvordan kan tryk ændre densiteten af faste stoffer væsker og gasser?
Næste artikelHvad er centrifugalreaktion?
 Varme artikler
Varme artikler
-
 Skies of blue:Genanvendelse af kulstofemissioner til nyttige kemikalier og reduktion af den globale …Tilførsel af proton øger CO-elektrosyntesen til produktion af acetat og flygtige fedtsyrer. Kredit:Pusan National University Hurtig global urbanisering har dramatisk ændret vores planets ansigt,
Skies of blue:Genanvendelse af kulstofemissioner til nyttige kemikalier og reduktion af den globale …Tilførsel af proton øger CO-elektrosyntesen til produktion af acetat og flygtige fedtsyrer. Kredit:Pusan National University Hurtig global urbanisering har dramatisk ændret vores planets ansigt, -
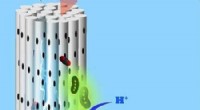 Hjælpsomme mikrober indånder kuldioxid gennem en porøs cylindrisk elektrode og udstråler nyttige…Mikrober, der vokser på porøse cylindriske elektroder, suger CO2 ind og omdanner det til nyttige kemikalier såsom acetat og metan. © 2018 Bin Bian Mikrober kan blive nøgleallierede i globale bestr
Hjælpsomme mikrober indånder kuldioxid gennem en porøs cylindrisk elektrode og udstråler nyttige…Mikrober, der vokser på porøse cylindriske elektroder, suger CO2 ind og omdanner det til nyttige kemikalier såsom acetat og metan. © 2018 Bin Bian Mikrober kan blive nøgleallierede i globale bestr -
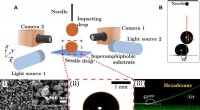 Løft af en siddende dråbe fra en superamfifob overflade ved hjælp af en stødende dråbeEksperimentel tilgang og det fastsiddende fald. (A) Skitse af den eksperimentelle opsætning for binær dråbepåvirkning på superamfifobe overflader. Nålen er fikseret for at indstille stødhøjden i Z-ret
Løft af en siddende dråbe fra en superamfifob overflade ved hjælp af en stødende dråbeEksperimentel tilgang og det fastsiddende fald. (A) Skitse af den eksperimentelle opsætning for binær dråbepåvirkning på superamfifobe overflader. Nålen er fikseret for at indstille stødhøjden i Z-ret -
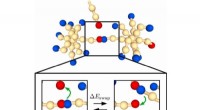 Produktion af genanvendeligt plastik et skridt nærmereDe stjerneformede polymerer bytter bindinger. Kredit:Eindhoven University of Technology En nyligt opdaget gruppe af genanvendelig plast ser ud til at være et lovende alternativ til den hårde plast
Produktion af genanvendeligt plastik et skridt nærmereDe stjerneformede polymerer bytter bindinger. Kredit:Eindhoven University of Technology En nyligt opdaget gruppe af genanvendelig plast ser ud til at være et lovende alternativ til den hårde plast


