Forklar hvorfor en gas ikke har nogen bestemt form og volumen?
1. Svage intermolekylære kræfter:
* Gasmolekyler er meget langt fra hinanden sammenlignet med væsker eller faste stoffer.
* De attraktive kræfter (intermolekylære kræfter) mellem gasmolekyler er meget svage.
* Dette betyder, at molekylerne har en masse frihed til at bevæge sig rundt.
2. Høj kinetisk energi:
* Gasmolekyler har høj kinetisk energi. De er i konstant, tilfældig bevægelse, der kolliderer med hinanden og væggene i deres beholder.
* Denne konstante bevægelse forhindrer dem i at forblive i en fast position eller arrangement.
3. Kompressibilitet:
* Fordi molekylerne er så langt fra hinanden, kan gasser let komprimeres.
* Når der påføres tryk, tvinges molekylerne tættere sammen, hvilket reducerer volumenet.
4. Udvidelse:
* Gasser kan udvide til at fylde enhver beholder, de besætter.
* Hvis du lægger en gas i en større beholder, spreder molekylerne sig for at besætte hele rummet.
Kortfattet: Kombinationen af svage intermolekylære kræfter, høj kinetisk energi og evnen til at komprimere og udvide betyder, at gasmolekyler konstant bevæger sig og ændrer deres positioner. Dette resulterer i, at gasser ikke har nogen fast form eller volumen. De tager formen og volumenet på deres beholder.
Sidste artikelHvad er forskellen mellem kemiske og fysiske egenskaber?
Næste artikelEr en plasticine -leder af varme?
 Varme artikler
Varme artikler
-
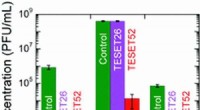 Selvsteriliserende polymer viser sig effektiv mod lægemiddelresistente patogenerKredit: Materialer Horisonter (2019). DOI:10.1039/C9MH00726A Forskere fra North Carolina State University har fundet ud af, at en elastisk polymer besidder bredspektrede antimikrobielle egenskabe
Selvsteriliserende polymer viser sig effektiv mod lægemiddelresistente patogenerKredit: Materialer Horisonter (2019). DOI:10.1039/C9MH00726A Forskere fra North Carolina State University har fundet ud af, at en elastisk polymer besidder bredspektrede antimikrobielle egenskabe -
 Vurdering af salens potentielle aktivitet mod proteiner af SARS-CoV-2Ifølge videnskabsmænd er salen - stoffet på billedet - relativt simpelt og billigt at syntetisere. Kredit:UrFU / Damir Safin Forskere fandt ud af, at salen effektivt er i stand til at binde en rækk
Vurdering af salens potentielle aktivitet mod proteiner af SARS-CoV-2Ifølge videnskabsmænd er salen - stoffet på billedet - relativt simpelt og billigt at syntetisere. Kredit:UrFU / Damir Safin Forskere fandt ud af, at salen effektivt er i stand til at binde en rækk -
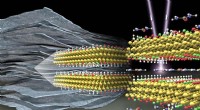 Hurtig og rasende:Ny klasse af 2D-materialer lagrer elektrisk energiMXener er 2D-materialer, der danner flerlagspartikler (venstre), som pseudokondensatorer er lavet af. Skinnende røntgenlys på MXener afslørede ændringer i deres kemiske struktur ved interkalation af u
Hurtig og rasende:Ny klasse af 2D-materialer lagrer elektrisk energiMXener er 2D-materialer, der danner flerlagspartikler (venstre), som pseudokondensatorer er lavet af. Skinnende røntgenlys på MXener afslørede ændringer i deres kemiske struktur ved interkalation af u -
 Venstre eller højre? Ny algoritme tager chiralitetsbestemmelse til næste niveauKredit:HIMS / RSC Forskere ved Molecular Photonics-gruppen under Van t Hoff Instituttet for Molekylær Videnskab ved Universitetet i Amsterdam har væsentligt forbedret den eksperimentelle bestemmel
Venstre eller højre? Ny algoritme tager chiralitetsbestemmelse til næste niveauKredit:HIMS / RSC Forskere ved Molecular Photonics-gruppen under Van t Hoff Instituttet for Molekylær Videnskab ved Universitetet i Amsterdam har væsentligt forbedret den eksperimentelle bestemmel
- Hvad er tre anvendelser til ilt?
- Hvilken type fundament er egnet til laterit jord?
- Hvem udviklede begrebet atomnummer?
- Hvordan afbalancerer man den kemiske ligning HBr H2 plus Br2 N2O N2 O2 CH4 CO2 H2O?
- Er blandingen af jod og ethanol en heterogen. eller homogen blanding?
- Forbrugerne viste sig at være mere åbne over for vedvarende energitillæg, hvis de mener, det er r…


