Hvad er et stof, der fremskynder reaktionen?
Her er en sammenbrud:
* katalysator: Et stof, der øger hastigheden for en kemisk reaktion uden at blive konsumeret i processen. Katalysatorer fungerer ved at tilvejebringe en alternativ reaktionsvej med en lavere aktiveringsenergi.
* Aktiveringsenergi: Den mindste mængde energi, der kræves for at en reaktion kan forekomme.
Eksempler på katalysatorer:
* enzymer: Biologiske katalysatorer, der fremskynder biokemiske reaktioner i levende organismer.
* Metaller: Mange metaller, som platin og nikkel, fungerer som katalysatorer i industrielle processer.
* syrer: Visse syrer kan katalysere reaktioner, som hydrolyse af estere.
nøglefunktioner ved katalysatorer:
* ikke konsumeret: De er ikke opbrugt under reaktionen.
* Nedre aktiveringsenergi: De giver en alternativ vej med mindre energi krævet.
* specifikt: Katalysatorer fungerer ofte for specifikke reaktioner eller typer af reaktioner.
* kan være homogen eller heterogen: Homogene katalysatorer er i den samme fase som reaktanterne (f.eks. Opløs i opløsning), mens heterogene katalysatorer er i en anden fase (f.eks. En solid katalysator i en flydende reaktion).
Fortæl mig, hvis du vil vide mere om katalysatorer eller deres specifikke applikationer!
Sidste artikelNår to atomer rører ved, hvordan kommunikeres det i kode?
Næste artikelTørre hurtige kemiske eller fysiske egenskaber?
 Varme artikler
Varme artikler
-
 Ny polymer kan øge ydeevnen af organiske og perovskit-solcellerVariation på forsiden af Macromolecular Chemistry and Physics-udgaven med undersøgelsen rapporteret i denne historie, begge kunstværker af undersøgelsens første forfatter. Kredit:Marina Tepliakova/S
Ny polymer kan øge ydeevnen af organiske og perovskit-solcellerVariation på forsiden af Macromolecular Chemistry and Physics-udgaven med undersøgelsen rapporteret i denne historie, begge kunstværker af undersøgelsens første forfatter. Kredit:Marina Tepliakova/S -
 Iagttager en skiftende platinelektrodeKredit:Leiden University Overfladen på platinelektroder ændrer sig meget mere under brug end tidligere antaget. I et samarbejde mellem Leiden Institutes of Chemistry and Physics, kemikere Leon Jac
Iagttager en skiftende platinelektrodeKredit:Leiden University Overfladen på platinelektroder ændrer sig meget mere under brug end tidligere antaget. I et samarbejde mellem Leiden Institutes of Chemistry and Physics, kemikere Leon Jac -
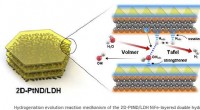 Dobbeltlagskatalysator genererer mere brintKredit:Yu-Rim Hong et al. Hydrogen-genererende katalysatorer kan skabe synergistiske effekter, når forskellige materialer er lagdelt med deres unikke egenskaber. For nylig har et koreansk forskerho
Dobbeltlagskatalysator genererer mere brintKredit:Yu-Rim Hong et al. Hydrogen-genererende katalysatorer kan skabe synergistiske effekter, når forskellige materialer er lagdelt med deres unikke egenskaber. For nylig har et koreansk forskerho -
 Molekylært tynd hybrid perovskit til avancerede optoelektroniske applikationerFigur 1:(a - e) Optisk billede af store 2D hybrid perovskitter (enkeltkrystal) og forskellige homologe serier (forbindelser med den samme funktionelle gruppe, men adskiller sig med antallet af gentagn
Molekylært tynd hybrid perovskit til avancerede optoelektroniske applikationerFigur 1:(a - e) Optisk billede af store 2D hybrid perovskitter (enkeltkrystal) og forskellige homologe serier (forbindelser med den samme funktionelle gruppe, men adskiller sig med antallet af gentagn
- På den amerikanske sædvanlige side af lineal, hvad er nummererede trin, der kaldes?
- Dobbelt Janus nanopartikler omdannet til kopformede dynamiske inklusionslegemer til kolloid design
- Nævn noget, der betragtes som stof?
- Hvad er tyngdekraften på jorden under en solformørkelse?
- Hvilken farve vender kobbersulfat den universelle indikator?
- Forskere lærer, hvorfor PSA-niveauer afspejler prostatacancerprogression


