Hvilken gas effuserer hurtigere ved den samme temperaturmolekylært ilt eller atomisk argon?
Grahams lov om effusion siger, at hastigheden for effusion af en gas er omvendt proportional med kvadratroden af dens molære masse.
molmasse:
* Oxygen (O₂):32 g/mol
* Argon (AR):40 g/mol
Beregning:
Forholdet mellem effusionshastigheder er givet af:
`` `
Effusionshastighed af O₂ / hastighed for effusion af AR =√ (molmasse af AR / molær masse af O₂)
=√ (40 g/mol/32 g/mol)
=√1.25
≈ 1.12
`` `
Dette betyder, at molekylært ilt effuserer cirka 1,12 gange hurtigere end atomargon på den samme temperatur.
Konklusion:
Da ilt har en lavere molær masse end argon, vil den effusere hurtigere på grund af dens højere gennemsnitlige hastighed.
 Varme artikler
Varme artikler
-
 Meget følsom trigger muliggør hurtig påvisning af biologiske agenserRapid Agent Aerosol Detector blev fotograferet med en 12-tommer lineal for at illustrere skalaen. Kredit:Massachusetts Institute of Technology Enhver plads, lukket eller åben, kan være sårbare ove
Meget følsom trigger muliggør hurtig påvisning af biologiske agenserRapid Agent Aerosol Detector blev fotograferet med en 12-tommer lineal for at illustrere skalaen. Kredit:Massachusetts Institute of Technology Enhver plads, lukket eller åben, kan være sårbare ove -
 Biosyntese af cyanobakterin åbner op for en ny klasse af naturlige forbindelser til anvendelse i me…Fermentering af cyanobakterier i en fotobioreaktor ved TU Dresden. Kredit:Prof. Tobias Gulder At naturen er en fremragende kemiker, demonstreres af den overflod af molekyler, såkaldte naturprodukte
Biosyntese af cyanobakterin åbner op for en ny klasse af naturlige forbindelser til anvendelse i me…Fermentering af cyanobakterier i en fotobioreaktor ved TU Dresden. Kredit:Prof. Tobias Gulder At naturen er en fremragende kemiker, demonstreres af den overflod af molekyler, såkaldte naturprodukte -
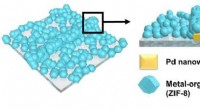 Ultrahurtig og ultrafølsom hydrogensensorRepræsentativt billede af dette papir udgivet i ACS Nano den 26. september Kredit:KAIST Et KAIST-team lavede en ultrahurtig hydrogensensor, der kan detektere hydrogengasniveauer under 1% på mind
Ultrahurtig og ultrafølsom hydrogensensorRepræsentativt billede af dette papir udgivet i ACS Nano den 26. september Kredit:KAIST Et KAIST-team lavede en ultrahurtig hydrogensensor, der kan detektere hydrogengasniveauer under 1% på mind -
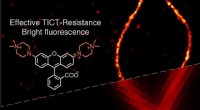 Oplyser vejen til superopløsningsbilleddannelse med forbedrede rhodaminfarvestofferForskere fra DUT og SUTD udviklede en ny klasse af kvaternære piperazin-substituerede rhodaminer med fremragende kvanteudbytter (Φ =0,93) og overlegen lysstyrke (ε × Φ =8,1 × 104 L·mol-1·cm-1), til bi
Oplyser vejen til superopløsningsbilleddannelse med forbedrede rhodaminfarvestofferForskere fra DUT og SUTD udviklede en ny klasse af kvaternære piperazin-substituerede rhodaminer med fremragende kvanteudbytter (Φ =0,93) og overlegen lysstyrke (ε × Φ =8,1 × 104 L·mol-1·cm-1), til bi
- Hvad hedder bjergkæden i Utah, der blev skabt af jordskælv?
- Hvordan fungerer antirustprodukter?
- Hvad er tre processer, som en metamorfe klippe skal opleve, før den kan blive sedimentær klippe?
- Hårfarve er giftigt – kan naturlige alternativer fås til at virke?
- Hvilke lag af jorden er unik blandt jordbaserede planeter?
- Er økologisk landbrug altid godt for miljøet? Forskere laver strategi for at hjælpe med at bestem…


