Hvad var de vigtigste bidrag til atomteorien?
Tidlige ideer:
* Democritus (460-370 f.Kr.): Selvom det ikke var baseret på eksperimentering, foreslog Democritus ideen om atomer som de grundlæggende, udelelige partikler, der udgør sagen. Han kaldte dem "atomoer", hvilket betyder "ukuttable."
* Aristoteles (384-322 f.Kr.): Aristoteles afviste Democritus 'idé og favoriserede begrebet fire elementer (jord, luft, ild og vand) som grundlag for alle stoffer. Dette synspunkt holdt sving i århundreder og forsinkede fremme af atomteori.
stigningen i eksperimentelle beviser:
* John Dalton (1803): Dalton formulerede sin atomteori baseret på eksperimentelle observationer. Hans vigtigste bidrag inkluderer:
* atomer er de grundlæggende byggesten til stof.
* atomer af et givet element er identiske i masse og egenskaber.
* atomer af forskellige elementer har forskellige masser og egenskaber.
* Kemiske reaktioner involverer omarrangement af atomer, ikke deres skabelse eller ødelæggelse.
* J.J. Thomson (1897): Thomson opdagede elektronet ved hjælp af et katodestrålerør. Dette beviste, at atomer ikke var udelelige, som Dalton havde troet. Han foreslog "blomme budding -modellen", hvor negativt ladede elektroner blev indlejret i en positivt ladet sfære.
* Ernest Rutherford (1911): Rutherford udførte det berømte guldfolieeksperiment, som viste, at det meste af atomets masse og positive ladning er koncentreret i en lille, tæt kerne. Dette førte til udviklingen af atomets nukleare model, hvor elektroner kredserede kernen.
* Niels Bohr (1913): Bohr foreslog en model af atomet, hvor elektroner kredsede kernen i specifikke, kvantiserede energiniveauer. Denne model forklarede de spektrale linjer, der blev udsendt af atomer, som ikke blev forklaret af Rutherfords model.
Den moderne atomteori:
* Erwin Schrödinger (1926): Udviklede bølgemekanisk model af atomet, hvor elektroner behandles som bølger snarere end partikler. Denne model giver en mere nøjagtig beskrivelse af atomadfærd og elektronfordeling inden for atomet.
* James Chadwick (1932): Opdagede neutronen, en neutral partikel, der er bosiddende i kernen. Dette tilføjede et andet stykke til puslespillet med atomstruktur.
Andre nøgleudviklinger:
* kvantemekanik: Udviklingen af kvantemekanik i begyndelsen af det 20. århundrede revolutionerede vores forståelse af atomet og afslørede den sandsynlige karakter af elektronadfærd og begrænsningerne i klassisk fysik i atomskalaen.
* isotoper: Opdagelsen af isotoper viste, at atomer af det samme element kan have forskellige antal neutroner, hvilket således varierer i masse.
* Subatomære partikler: Yderligere forskning førte til opdagelsen af adskillige subatomære partikler, såsom kvarker, gluoner og bosoner, hvilket afslørede kompleksiteten af atomets interne struktur.
nøglepunkter at huske:
* atomteori har udviklet sig gennem århundreder. Det startede med filosofiske ideer og gik videre gennem eksperimentelle opdagelser.
* Det er en løbende proces. Forskere fortsætter med at udforske atomet og afslører nye detaljer om dets struktur og opførsel.
* atomteori er grundlaget for moderne kemi og fysik. Det hjælper os med at forstå verden omkring os på det mest grundlæggende niveau.
Sidste artikelHvad er radioaktive atomer?
Næste artikelHvor mange valenselektroner har promethium?
 Varme artikler
Varme artikler
-
 Forskere opdager forbindelser, der kunne have været med til at starte liv på JordenFosforatomer i gult, iltatomer indblandet. Kredit:Britvin et al / Geology, 2020 Fosfor er et element, der er afgørende for livet. Det er grundlæggende for alle levende organismer, og er en nøgleko
Forskere opdager forbindelser, der kunne have været med til at starte liv på JordenFosforatomer i gult, iltatomer indblandet. Kredit:Britvin et al / Geology, 2020 Fosfor er et element, der er afgørende for livet. Det er grundlæggende for alle levende organismer, og er en nøgleko -
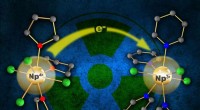 Åbner adgang til at udforske neptuniums syntetiske kemiEn ny, let fremstillet udgangsmateriale (til venstre) indeholdende neptunium (Np3+) kan let fremstilles ved en elektron (e-) overførsel til en moder neptunium (Np4+) forbindelse (højre). Denne proces
Åbner adgang til at udforske neptuniums syntetiske kemiEn ny, let fremstillet udgangsmateriale (til venstre) indeholdende neptunium (Np3+) kan let fremstilles ved en elektron (e-) overførsel til en moder neptunium (Np4+) forbindelse (højre). Denne proces -
 Forskere klemmer katalysatorer inde i værtsmaterialer som et skib i en flaskeVed hjælp af termodynamiske Pourbaix-diagrammer, videnskabsmænd kan presse katalysatorer inde i værtsmaterialer som et skib i en flaske. Kredit:Jingwei Hou Forskere ved Queen Mary University of Lo
Forskere klemmer katalysatorer inde i værtsmaterialer som et skib i en flaskeVed hjælp af termodynamiske Pourbaix-diagrammer, videnskabsmænd kan presse katalysatorer inde i værtsmaterialer som et skib i en flaske. Kredit:Jingwei Hou Forskere ved Queen Mary University of Lo -
 At finde træalternativer til truet ibenholtEn violin med et gribebræt lavet af schweizisk ibenholt. Kredit:Wilhelm Geigenbau AG, Suhr Ligesom mange tropiske træsorter, ibenholt er en truet art, der er vanskelig at bruge, sådan i instrument
At finde træalternativer til truet ibenholtEn violin med et gribebræt lavet af schweizisk ibenholt. Kredit:Wilhelm Geigenbau AG, Suhr Ligesom mange tropiske træsorter, ibenholt er en truet art, der er vanskelig at bruge, sådan i instrument
- Hvilke to ting ville ske med dyr, hvis der ikke var nogen fotosyntese?
- Hvilket instrument måler massen af en pin?
- Er hydrogenperoxid et godt reduktionsmiddel?
- Brug af maskinlæring til at opdage softwaresårbarheder
- Er syrer fra planter rødder, der bryder klipper en mekanisk reaktion?
- Populært værktøj brugt af biologer til at prøve økosystemer?


