Hvorfor er ledning i gas langsomt?
1. Lav tæthed: Gasmolekyler er langt fra hinanden sammenlignet med væsker eller faste stoffer. Dette betyder, at der er færre kollisioner mellem molekyler, som er vigtige for at overføre varmeenergi.
2. Svage intermolekylære kræfter: Gasmolekyler har meget svage attraktive kræfter mellem dem. Det betyder, at det er mindre sandsynligt, at de deler kinetisk energi gennem kollisioner.
3. Høj gennemsnitlig fri sti: Den gennemsnitlige frie sti eller den gennemsnitlige afstand, som et molekyle bevæger sig, før den kolliderer med en anden, er meget længere i gasser end i væsker eller faste stoffer. Dette betyder, at der er færre muligheder for energioverførsel gennem kollisioner.
4. Dårlig termisk ledningsevne: Gasser har generelt lav termisk ledningsevne, hvilket betyder, at de er dårlige til at overføre varme. Dette er på grund af de faktorer, der er nævnt ovenfor - svage intermolekylære kræfter, lav densitet og lang gennemsnitlig fri sti.
5. Langsom energioverførsel: Når kollisioner forekommer, er energioverførslen mellem gasmolekyler mindre effektiv end i væsker eller faste stoffer. Dette skyldes, at molekylerne bevæger sig hurtigere og har en kortere interaktionstid.
Eksempel: Forestil dig at prøve at passere en bold ned ad en række mennesker. Hvis folket er langt fra hinanden og ikke holder hænder, vil bolden tage meget længere tid at nå slutningen af linjen. Dette svarer til, hvordan varmeledning fungerer i gasser. Molekylerne er langt fra hinanden og er ikke stærkt forbundet, hvilket gør energioverførslen langsom.
Kortfattet: Den lave densitet, svage intermolekylære kræfter, lang gennemsnitlig fri sti og langsom energioverførsel mellem molekyler i gasser bidrager alle til deres dårlige termiske ledningsevne og langsom ledning af varme.
 Varme artikler
Varme artikler
-
 Forbrændingsadfærd af aromater kan være nøglen til at forbedre udvindingen af tung olieAbstrakt resumé. Kredit:Kazan Federal University Problemet med olieudtømning bliver mere og mere relevant hver dag. Efterhånden som der opstår underskud, ikke-traditionelle og tunge olier, herunde
Forbrændingsadfærd af aromater kan være nøglen til at forbedre udvindingen af tung olieAbstrakt resumé. Kredit:Kazan Federal University Problemet med olieudtømning bliver mere og mere relevant hver dag. Efterhånden som der opstår underskud, ikke-traditionelle og tunge olier, herunde -
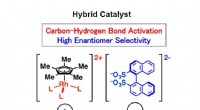 Hybrid katalysator med høj enantiomer selektivitetHybridkatalysatoren er dannet ved at kombinere en enkelt struktureret, kommercielt tilgængeligt rhodium og en let tilgængelig organisk katalysator gennem ioniske interaktioner. Kredit:Hokkaido Univers
Hybrid katalysator med høj enantiomer selektivitetHybridkatalysatoren er dannet ved at kombinere en enkelt struktureret, kommercielt tilgængeligt rhodium og en let tilgængelig organisk katalysator gennem ioniske interaktioner. Kredit:Hokkaido Univers -
 Makerspaces kunne muliggøre udbredt anvendelse af mikrofluidikMikrofluidiske enheder til at udføre forskellige assays blev skabt med værktøjerne i Lincoln Laboratorys Technology Office Innovation Laboratory. Kredit:Nicole Fandel I mere end et årti, videnskab
Makerspaces kunne muliggøre udbredt anvendelse af mikrofluidikMikrofluidiske enheder til at udføre forskellige assays blev skabt med værktøjerne i Lincoln Laboratorys Technology Office Innovation Laboratory. Kredit:Nicole Fandel I mere end et årti, videnskab -
 Afkodning af materialeslitage med supercomputereEt lille stykke metal simuleres på en computer - atom for atom. Kredit:TU Wien Slid og friktion er afgørende spørgsmål i mange industrisektorer:Hvad sker der, når en overflade glider hen over en a
Afkodning af materialeslitage med supercomputereEt lille stykke metal simuleres på en computer - atom for atom. Kredit:TU Wien Slid og friktion er afgørende spørgsmål i mange industrisektorer:Hvad sker der, når en overflade glider hen over en a
- Varmere klima fører til aktuelle tendenser til social uro og massemigration:undersøgelse
- Når du tilføjer calciumcarbonat til muldjord, hvorfor forhindrer det i at blive sur?
- Hvad sker der med lydvolumenet, når energi stiger?
- Hvilke andre fysiske mængder kvantificeres bortset fra opladning?
- Franske Renault-arbejdere er uberørte, da administrerende direktør Ghosn står over for en retssag…
- Hvor lang tid i tommer er 20 mm?


