En positivt ladet partikel af et element som NA og CA?
Her er hvorfor:
* atomer er neutrale: Atomer har normalt et lige antal protoner (positivt ladede) og elektroner (negativt ladet), hvilket gør dem elektrisk neutrale.
* taber elektroner: Når et atom mister en eller flere elektroner, bliver det positivt ladet, fordi det nu har flere protoner end elektroner.
* kationer: Disse positivt ladede atomer kaldes kationer.
Eksempler:
* natrium (NA): Et neutralt natriumatom har 11 protoner og 11 elektroner. Hvis det mister en elektron, bliver det en natriumkation (Na+) med 11 protoner og 10 elektroner.
* calcium (CA): Et neutralt calciumatom har 20 protoner og 20 elektroner. Hvis det mister to elektroner, bliver det en calciumkation (Ca2+) med 20 protoner og 18 elektroner.
Dannelse af kationer:
Kationer dannes ofte, når metaller reagerer med ikke -metaller. Metaller har en tendens til at miste elektroner lettere end ikke -metaller. Dette skyldes deres elektronkonfiguration og det faktum, at de generelt har lavere elektronegativitet (tiltrækning for elektroner).
 Varme artikler
Varme artikler
-
 Beetle-vægte holder hemmeligheden bag at skabe bæredygtig maling af genbrugsplastik, forskning vis…Foto af to cyphochilus biller. Kredit:Olimpia1lli - CC BY-SA 4.0 Strukturen af ultrahvide billevægte kunne være nøglen til at fremstille lyshvid bæredygtig maling ved hjælp af genbrugsplastikaff
Beetle-vægte holder hemmeligheden bag at skabe bæredygtig maling af genbrugsplastik, forskning vis…Foto af to cyphochilus biller. Kredit:Olimpia1lli - CC BY-SA 4.0 Strukturen af ultrahvide billevægte kunne være nøglen til at fremstille lyshvid bæredygtig maling ved hjælp af genbrugsplastikaff -
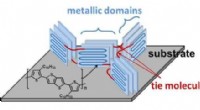 Uvridende plastik til opladning af Internet-of-Things-enhederTil venstre:Forskerne fandt ud af, at deres dopingteknik dannede bindinger (røde) mellem PBTTTs krystallinske dele (blå rektangler). Til højre:De fandt også ud af, at PBTTT var snoet i sin naturlige t
Uvridende plastik til opladning af Internet-of-Things-enhederTil venstre:Forskerne fandt ud af, at deres dopingteknik dannede bindinger (røde) mellem PBTTTs krystallinske dele (blå rektangler). Til højre:De fandt også ud af, at PBTTT var snoet i sin naturlige t -
 Forskere indser ideel kagome metal elektronisk strukturDenne illustration viser det karakteristiske sheriff star-type mønster af Fermi overfladen, eller fordeling af elektronenergi og momentum, for kagome-metallet FeSn, en 1-til-1-forbindelse af jern og t
Forskere indser ideel kagome metal elektronisk strukturDenne illustration viser det karakteristiske sheriff star-type mønster af Fermi overfladen, eller fordeling af elektronenergi og momentum, for kagome-metallet FeSn, en 1-til-1-forbindelse af jern og t -
 Forskere udvikler tilgang til vedvarende energi til fremstilling af ammoniakWilliam Schneider. Kredit:University of Notre Dame Forskere ved University of Notre Dame udvikler en tilgang til vedvarende energi til at syntetisere ammoniak, en væsentlig komponent af gødning, d
Forskere udvikler tilgang til vedvarende energi til fremstilling af ammoniakWilliam Schneider. Kredit:University of Notre Dame Forskere ved University of Notre Dame udvikler en tilgang til vedvarende energi til at syntetisere ammoniak, en væsentlig komponent af gødning, d
- Hvordan overlever insekter i tropisk klima?
- Hvad er den komplette ioniske ligning for reaktion mellem Na2SO4 og CaCl2?
- Er der to typer subatomære partikler kaldet elektroner og ioner i kernen?
- Udforsk Merkur i en ny bog
- Hvor mange stjerner er der i svanen Cygnus?
- Hvordan hopper en glasbold og ikke bremser?


