Hvilken type organisk sammensat modsiger omdømme som et universelt opløsningsmiddel?
Den type organisk forbindelse, der modsiger dette omdømme, er ikke-polære organiske forbindelser .
Her er hvorfor:
* vand er et polært molekyle: Dette betyder, at det har en positiv og negativ ende på grund af den ujævne deling af elektroner mellem ilt- og brintatomer. Denne polaritet giver vand mulighed for at interagere stærkt med andre polære molekyler og ioniske forbindelser og opløser dem.
* Ikke-polære organiske forbindelser mangler ladningsadskillelse: De har en jævn fordeling af elektroner, hvilket gør dem ude af stand til at danne stærke interaktioner med polære vandmolekyler.
Eksempler på ikke-polære organiske forbindelser inkluderer:
* olier og fedt: Disse består af lange kæder af kulbrinter, som er ikke-polære. Dette er grunden til, at olie og vand ikke blandes.
* voks: I lighed med olier og fedt er voks ikke-polære og uopløselige i vand.
Derfor er ikke-polære organiske forbindelser ikke opløselige i vand og modsiger forestillingen om, at vand er et universelt opløsningsmiddel .
Sidste artikelStartmolekyle af elektrontransportkæde?
Næste artikelHvilke kemikalier er der i tobak?
 Varme artikler
Varme artikler
-
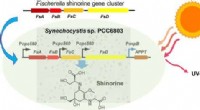 Gør dig klar til sommersolen med grønne solcremerKredit:American Chemical Society Selvom det har været en hård vinter for mange mennesker i USA, sommeren kommer. Og det betyder baggårdsgrill, sjov på stranden og selvfølgelig, sladder på solcreme
Gør dig klar til sommersolen med grønne solcremerKredit:American Chemical Society Selvom det har været en hård vinter for mange mennesker i USA, sommeren kommer. Og det betyder baggårdsgrill, sjov på stranden og selvfølgelig, sladder på solcreme -
 Polymer termisk regulator omdannes fra leder til isolator og tilbage igenDen rotationsforstyrrede sekskantede fase. Kredit:College of Engineering Polymerer bruges til at udvikle forskellige materialer, såsom plastik, nylon og gummi. I deres mest grundlæggende form, de
Polymer termisk regulator omdannes fra leder til isolator og tilbage igenDen rotationsforstyrrede sekskantede fase. Kredit:College of Engineering Polymerer bruges til at udvikle forskellige materialer, såsom plastik, nylon og gummi. I deres mest grundlæggende form, de -
 Strukturelle farver, uden glimmerDenne legetøjsdinosaur blev malet med en ny type ikke-iriserende strukturel farve. Kredit:Dongpeng Yang Strukturelle farver, som dem, der findes i nogle sommerfugles vinger, fugles fjer og billers
Strukturelle farver, uden glimmerDenne legetøjsdinosaur blev malet med en ny type ikke-iriserende strukturel farve. Kredit:Dongpeng Yang Strukturelle farver, som dem, der findes i nogle sommerfugles vinger, fugles fjer og billers -
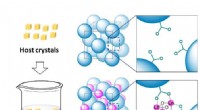 Den nemme måde at få et firkantet tilbud påFig. 1 En skematisk illustration af postsyntetisk dannelse af lanthanidhydroxid-klynge i værtskrystallerne. Kredit:Osaka University Forskere ved Osaka University har opdaget en ny metode til let a
Den nemme måde at få et firkantet tilbud påFig. 1 En skematisk illustration af postsyntetisk dannelse af lanthanidhydroxid-klynge i værtskrystallerne. Kredit:Osaka University Forskere ved Osaka University har opdaget en ny metode til let a
- Hvordan er lysår og astronomiske enheder ens?
- Hvordan spiser astronauter i rummet?
- Sø skabt af kulaffaldsskred oversvømmer den bosniske motorvej
- Hvad er en sac -svampe?
- Er den temperatur, hvormed en væske og faste stoftilstande er i ligevægt, er den samme som smeltep…
- Hvilken type pladegrænse er Carlsbad -huler i?


