Hvad er forskellen mellem et organisk kemikalie og uorganisk kemikalie?
organiske kemikalier:
* indeholder kulstof (c) som en primær komponent: Dette er den definerende egenskab.
* indeholder ofte brint (H): Selvom det ikke altid er til stede, findes brint ofte i organiske molekyler.
* indeholder ofte andre elementer: Disse elementer er typisk ikke -metaller som ilt (O), nitrogen (N), svovl (er), fosfor (P) og halogener.
* Form kovalente obligationer: Organiske molekyler holdes sammen af stærke kovalente bindinger.
* enorm strukturel kompleksitet: Organisk kemi er kendetegnet ved dannelsen af lange kæder, ringe og komplekse strukturer.
* afledt typisk fra levende organismer: Mange organiske forbindelser findes i planter og dyr.
Eksempler: Sukker, proteiner, fedt, olier, plast, naturgas, olie
uorganiske kemikalier:
* mangler kulstof som en primær komponent: Mens nogle uorganiske forbindelser kan indeholde kulstof, betragtes de ikke som organiske.
* bred vifte af elementer: Uorganiske forbindelser kan indeholde enhver kombination af elementer.
* involverer typisk ioniske bindinger: Mange uorganiske forbindelser dannes ved overførsel af elektroner mellem atomer, hvilket resulterer i ioniske bindinger.
* enklere strukturer: Uorganiske forbindelser har generelt enklere strukturer end organiske forbindelser.
* fundet i jordens skorpe, atmosfære og oceaner: Mange uorganiske forbindelser forekommer naturligt.
Eksempler: Vand (H₂O), salt (NaCl), kuldioxid (co₂), metaller (jern, guld), mineraler
Nøglepunkt: Forskellen mellem organisk og uorganisk kemi er ikke absolut. Nogle forbindelser, som kuldioxid (CO₂), kan betragtes som begge. Imidlertid giver de generelle principper beskrevet ovenfor en nyttig måde at skelne mellem de to kategorier.
 Varme artikler
Varme artikler
-
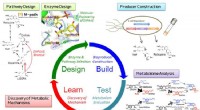 Konstruerede smarte celler forbedrer produktionen af farmaceutiske råvarerFigur 1 - Et design, Byg, Prøve, Lær workflow aktiveret forbedring af alkaloidproduktion. Kredit:Kobe University Forskere i Japan har udviklet et integreret syntetisk biologisk system til at konst
Konstruerede smarte celler forbedrer produktionen af farmaceutiske råvarerFigur 1 - Et design, Byg, Prøve, Lær workflow aktiveret forbedring af alkaloidproduktion. Kredit:Kobe University Forskere i Japan har udviklet et integreret syntetisk biologisk system til at konst -
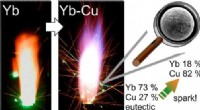 Forskere bruger sjældne jordarters metaller i legeringspulvere til at producere grønne, iøjnefald…Grafisk abstrakt. Kredit:ACS Omega (2022). DOI:10.1021/acsomega.2c03081 Stjernekastere kan være meget sjove - glimtende, brusende og spyttede lysbuer ud fra håndholdte pinde eller rør på jorden. Me
Forskere bruger sjældne jordarters metaller i legeringspulvere til at producere grønne, iøjnefald…Grafisk abstrakt. Kredit:ACS Omega (2022). DOI:10.1021/acsomega.2c03081 Stjernekastere kan være meget sjove - glimtende, brusende og spyttede lysbuer ud fra håndholdte pinde eller rør på jorden. Me -
 Nær-infrarøde reflekterende blandingsbelægninger har bedre optisk og køleydelseKredit:DOI:10.1016/j.solener.2021.06.061 Kinesiske forskere fandt for nylig, at en nær-infrarød reflekterende blandingscoating havde bedre optisk og køleydelse, derved reducerer den absorberede en
Nær-infrarøde reflekterende blandingsbelægninger har bedre optisk og køleydelseKredit:DOI:10.1016/j.solener.2021.06.061 Kinesiske forskere fandt for nylig, at en nær-infrarød reflekterende blandingscoating havde bedre optisk og køleydelse, derved reducerer den absorberede en -
 Nye lim klæber nemt, holder godt, og er en gas at trække fra hinandenNicholas Blelloch, Guarini 21, viser en midlertidig lim frem, der er stærk nok til at holde en ph.d.-kandidat, men kan frigives uden magt. Til dette foto, limen blev påført mellem karabinhagerne på to
Nye lim klæber nemt, holder godt, og er en gas at trække fra hinandenNicholas Blelloch, Guarini 21, viser en midlertidig lim frem, der er stærk nok til at holde en ph.d.-kandidat, men kan frigives uden magt. Til dette foto, limen blev påført mellem karabinhagerne på to
- Hvad er uorganisk kolloid?
- Amerikanske embedsmænd:Arktisk optøning giver anledning til bekymring for national sikkerhed
- Hvad forventes jordtilstandens elektronkonfiguration for beryllium?
- Kan Kodak redde sig selv via en patentbonanza?
- Hvilken organel frigiver energi til metabolisk aktivitet i en nervecelle?
- Sådan beregnes en Rate Constant


