Ikke -polære opløsningsmidler vil let opløse faste stoffer, der er?
Her er hvorfor:
* "som opløser som" :Dette er et grundlæggende princip i kemi. Opløsningsmidler har en tendens til at opløse opløsninger, der har lignende polariteter.
* polaritet :Polære molekyler har en ujævn fordeling af ladning, hvilket skaber en positiv og negativ ende. Ikke -polære molekyler har en jævn fordeling af ladning.
* Intermolekylære kræfter :Ikke -polære opløsningsmidler og opløste stoffer interagerer primært gennem svage London -spredningskræfter. Disse kræfter er mere tilbøjelige til at danne mellem molekyler med lignende polariteter.
Eksempler:
* ikke -polær opløsningsmiddel: Hexan (C6H14)
* ikke -polært fast stof :Naphthalen (C10H8)
I modsætning hertil :
* polært opløsningsmiddel: Vand (H2O)
* polært fast stof :Sukker (C12H22O11)
Vand ville opløse sukker godt, fordi begge er polære. Hexan ville opløse naphthalen godt, fordi begge er ikke -polære.
 Varme artikler
Varme artikler
-
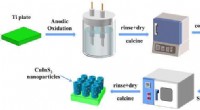 CuInS2/TiO2-fotoanodekompositter klarer sig godt i foto-induceret katodisk beskyttelseGrafisk abstrakt. Kredit:Journal of Materials Science &Technology (2022). DOI:10.1016/j.jmst.2022.02.011 Fotogenereret katodisk beskyttelsesteknologi som en værdifuld gren af fotokatalyse og foto
CuInS2/TiO2-fotoanodekompositter klarer sig godt i foto-induceret katodisk beskyttelseGrafisk abstrakt. Kredit:Journal of Materials Science &Technology (2022). DOI:10.1016/j.jmst.2022.02.011 Fotogenereret katodisk beskyttelsesteknologi som en værdifuld gren af fotokatalyse og foto -
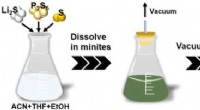 Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele
Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele -
 Kollagen nanofibriller i pattedyrs væv bliver stærkere med træningEn kollagenfibril monteret på en MEMS mekanisk testanordning. Nederst er et enkelt menneskehår til størrelsessammenligning. Kredit:University of Illinois Department of Aerospace Engineering Kollag
Kollagen nanofibriller i pattedyrs væv bliver stærkere med træningEn kollagenfibril monteret på en MEMS mekanisk testanordning. Nederst er et enkelt menneskehår til størrelsessammenligning. Kredit:University of Illinois Department of Aerospace Engineering Kollag -
 Klæbende situation:Ny proces forvandler trærester til tapeIllustration, der repræsenterer transformationen af træer til tape. Ingeniører ved University of Delaware har udviklet en ny proces til at lave tape af en vigtig bestanddel af træer og planter kalde
Klæbende situation:Ny proces forvandler trærester til tapeIllustration, der repræsenterer transformationen af træer til tape. Ingeniører ved University of Delaware har udviklet en ny proces til at lave tape af en vigtig bestanddel af træer og planter kalde
- Disney øger sit bud på Fox for at imødegå Comcast
- Startup kommercialiserer MRI-enheder, der kan forbedre medicinsk diagnostik
- Satellitter øjentyfon Vongfong landfald i Filippinerne
- De første af deres slags billeder kunne hjælpe med at bruge DNA til at bygge nanoskala-enheder
- Undersøgelse sporer hjernens indre funktion med ny biosensor
- Nævn tre partikelacceleratorer i USA og beskriv hvilken type eksperimenter hver accelerator er desi…


