Kulilte i vand:Opløselighed, reaktioner og ligevægt
* Lav opløselighed: CO er kun lidt opløseligt i vand. Det betyder, at kun en lille mængde CO vil opløses på et givet tidspunkt.
* Ingen væsentlig kemisk reaktion: CO reagerer ikke væsentligt med vand for at danne nye kemiske arter. I modsætning til gasser som kuldioxid (CO2), der danner kulsyre (H2CO3) i vand, gennemgår CO ikke en lignende reaktion.
* Ligevægt: Den opløste CO eksisterer i ligevægt med CO i gasfasen. Når koncentrationen af CO i vandet falder, vil mere CO fra gasfasen opløses for at genoprette ligevægten.
Men CO's interaktion med vand er ikke helt ubetydelig:
* Hemoglobinbinding: CO er kendt for at binde til hæmoglobin i blodet, selv når det er opløst i vand. Denne binding er langt stærkere end oxygens binding til hæmoglobin, hvilket fører til kulilteforgiftning.
* Potentiale for hydrolyse: Under ekstremt specifikke forhold kan CO reagere med vand i nærværelse af stærke katalysatorer, men dette er ikke en almindelig begivenhed.
Opsummering: Mens CO opløses i vand i ringe grad, er dets interaktion med vand svag og resulterer ikke i væsentlige kemiske reaktioner. Den mest bemærkelsesværdige konsekvens af CO-opløsning i vand er dets potentiale til at binde sig til hæmoglobin og forårsage forgiftning.
Sidste artikelForstå bufferopløsninger:syrer, baser og salte
Næste artikelAtomer vs. ioner:Forstå forskellen
 Varme artikler
Varme artikler
-
 Forskere udvikler billig chip til at detektere tilstedeværelse og mængde af COVID-19 antistofferAntistoftestplatformen, udviklet af forskere fra Micro/Bio/Nanofluidics Unit på OIST. Kredit:OIST Robust og udbredt antistoftest er fremstået som en nøglestrategi i kampen mod SARS-CoV-2, den viru
Forskere udvikler billig chip til at detektere tilstedeværelse og mængde af COVID-19 antistofferAntistoftestplatformen, udviklet af forskere fra Micro/Bio/Nanofluidics Unit på OIST. Kredit:OIST Robust og udbredt antistoftest er fremstået som en nøglestrategi i kampen mod SARS-CoV-2, den viru -
 Fra orkaner til jordskælv, rumstationseksperiment overvinder udfordringerCamila Morales-Navas udfører de sidste forberedelser på det elektrokemiske ammoniakfjernelsessystem forud for parabolflyvningstest. Kredit:University of Puerto Rico Pladsen er hård, ordsproget sig
Fra orkaner til jordskælv, rumstationseksperiment overvinder udfordringerCamila Morales-Navas udfører de sidste forberedelser på det elektrokemiske ammoniakfjernelsessystem forud for parabolflyvningstest. Kredit:University of Puerto Rico Pladsen er hård, ordsproget sig -
 Revneformering er asymmetrisk i polære materialerKredit:Catalan Institute of Nanoscience and Nanotechnology ICN2 Oxide Nanophysics Group, ledet af ICREA prof. Gustau Catalán, har udgivet i Fysiske anmeldelsesbreve hvordan, på grund af flexoele
Revneformering er asymmetrisk i polære materialerKredit:Catalan Institute of Nanoscience and Nanotechnology ICN2 Oxide Nanophysics Group, ledet af ICREA prof. Gustau Catalán, har udgivet i Fysiske anmeldelsesbreve hvordan, på grund af flexoele -
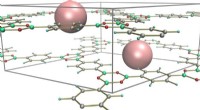 Porøse polymerer viser bemærkelsesværdig stabilitet ved højt trykPorøst nanomateriale kaldet COFer (kovalente organiske rammer). Kredit:Alexandr Talyzin Umeå-fysikere i samarbejde med Dresdens Tekniske Universitet og Chalmers Universitet er de første til at vis
Porøse polymerer viser bemærkelsesværdig stabilitet ved højt trykPorøst nanomateriale kaldet COFer (kovalente organiske rammer). Kredit:Alexandr Talyzin Umeå-fysikere i samarbejde med Dresdens Tekniske Universitet og Chalmers Universitet er de første til at vis
- Beskriv måder, hvorpå bevægende vand kan skære et landskab?
- Hvad er forskellen mellem et plante dyr og bakterieceller?
- Liste over atomteorierne
- Super-Kamiokande får en opgradering til at se neutrinoer fra gamle supernovaer
- Hvad er den temperatur, hvormed en flydende og gasformig faser er i ligevægt?
- Sådan fungerer haglgeværer


