Saltsyrestandardisering ved hjælp af borax:En detaljeret vejledning
Standardisering af saltsyre med borax
Introduktion:
Standardisering er processen med at bestemme den præcise koncentration af en opløsning, såsom saltsyre (HCl). Borax (natriumtetraboratdecahydrat, Na₂B₄O₇·10H₂O) er en primær standard, hvilket betyder, at det er en meget ren, stabil forbindelse, der kan vejes nøjagtigt og bruges til at bestemme koncentrationen af en anden opløsning. Denne metode er baseret på reaktionen mellem borax og HCl, som producerer en svag syre (borsyre) og et salt (natriumchlorid).
Procedure:
1. Forberedelse af boraxopløsning:
- Vej nøjagtigt ca. 2,0 g borax (Na₂B₄O₇·10H₂O) og opløs det i ca. 100 ml destilleret vand.
- Overfør opløsningen kvantitativt til en 250 ml målekolbe og fyld op til mærket med destilleret vand.
- Beregn den nøjagtige koncentration af boraxopløsningen (Molaritet).
2. Titrering:
- Fyld en burette med HCl-opløsningen, der skal standardiseres.
- Pipetter 25,00 ml af boraxopløsningen til en konisk kolbe.
- Tilføj et par dråber af en passende indikator som methylorange eller bromocresolgrøn.
- Titrer boraxopløsningen med HCl-opløsningen, indtil slutpunktet er nået (indikatorens farveændring).
- Optag mængden af brugt HCl.
- Gentag titreringen mindst to gange mere for at sikre nøjagtige resultater.
Beregninger:
1. Reaktionsstøkiometri:
Reaktionen mellem borax og HCl er:
Na2B4O7·10H2O + 2HCl → 4H3BO3 + 2NaCl + 5H2O
Ud fra denne ligning kan du se, at 1 mol borax reagerer med 2 mol HCl.
2. Beregning af HCl-koncentration:
- Beregn det gennemsnitlige volumen af HCl anvendt i titreringen.
- Brug følgende formel:
Molaritet af HCl =(Molaritet af borax × Volumen af borax × 2) / Volumen af HCl
Eksempel:
- Antag, at du brugte 2,00 g borax til at fremstille en 250 ml opløsning. Den molære masse af borax er 381,37 g/mol.
- Molariteten af boraxopløsningen er:2,00 g / 381,37 g/mol / 0,250 L =0,0210 M.
- Du titrerede 25,00 mL af boraxopløsningen og brugte i gennemsnit 23,45 mL HCl.
- HCl-opløsningens molaritet er:(0,0210 M × 25,00 mL × 2) / 23,45 mL =0,0447 M .
Sikkerhedsforanstaltninger:
- Bær altid passende beskyttelsesbriller og handsker ved håndtering af kemikalier.
- Arbejd i et godt ventileret område.
- Håndter saltsyre forsigtigt, da det er ætsende.
- Bortskaf kemikalier korrekt.
Bemærk: Dette er en grundlæggende oversigt over standardiseringsprocessen. Specifikke instruktioner og sikkerhedsforanstaltninger kan variere afhængigt af laboratoriet og det tilgængelige udstyr. Det er vigtigt at konsultere din laboratoriemanual eller din instruktør for detaljerede procedurer og sikkerhedsretningslinjer.
Sidste artikelForståelse af pH i destilleret vand:En neutral forklaring
Næste artikelOxidationstal af Br₂:En klar forklaring
 Varme artikler
Varme artikler
-
 Video:Små formskiftende polymerer udviklet til potentielle medicinske anvendelserKredit:Unsplash/CC0 Public Domain Ingeniører hos Caltech har udviklet en proces til generering af tredimensionelle arkitekterede polymerer med varmeafhængige formhukommelses egenskaber:Det vil sig
Video:Små formskiftende polymerer udviklet til potentielle medicinske anvendelserKredit:Unsplash/CC0 Public Domain Ingeniører hos Caltech har udviklet en proces til generering af tredimensionelle arkitekterede polymerer med varmeafhængige formhukommelses egenskaber:Det vil sig -
 Kubeformede jern-svovl-klynger understøtter multiple bindinger mellem jern og nitrogenKredit:Wiley I en række biologiske processer, jern-svovlklynger spiller en afgørende rolle, hvor de fungerer som cofaktorer til enzymer. Forskning offentliggjort i Angewandte Chemie viser nu, at
Kubeformede jern-svovl-klynger understøtter multiple bindinger mellem jern og nitrogenKredit:Wiley I en række biologiske processer, jern-svovlklynger spiller en afgørende rolle, hvor de fungerer som cofaktorer til enzymer. Forskning offentliggjort i Angewandte Chemie viser nu, at -
 Video:Hvordan kommunikerer planter med hinanden?Kredit:The American Chemical Society Forår er i luften! Det er tid til at slå græsplænen og indånde duften af nyslået græs. Men denne behagelige forårsduft kan faktisk være et kemisk råb om hjæ
Video:Hvordan kommunikerer planter med hinanden?Kredit:The American Chemical Society Forår er i luften! Det er tid til at slå græsplænen og indånde duften af nyslået græs. Men denne behagelige forårsduft kan faktisk være et kemisk råb om hjæ -
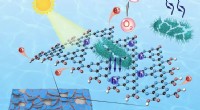 Forskere udvikler metalfri fotokatalysator til at rense patogenrigt vand på få minutterDe elektronoptagende grupper blev selektivt indført på kanten af g-C3N4 nanosheets til en fotodesinfektion. Kredit:TENG Zhenyuan og YANG Nailiang Forskere rundt om i verden har ødelagt deres hje
Forskere udvikler metalfri fotokatalysator til at rense patogenrigt vand på få minutterDe elektronoptagende grupper blev selektivt indført på kanten af g-C3N4 nanosheets til en fotodesinfektion. Kredit:TENG Zhenyuan og YANG Nailiang Forskere rundt om i verden har ødelagt deres hje


