Natrium-klorbindingsdannelse:Forståelse af ionisk binding og bordsalt (NaCl)
* Natrium (Na): Natrium har en elektron i sin yderste skal. Den ønsker at miste denne elektron for at opnå en stabil elektronkonfiguration som ædelgasserne.
* Klor (Cl): Klor har syv elektroner i sin yderste skal. Den ønsker at få en elektron for at opnå en stabil elektronkonfiguration som ædelgasserne.
Børsen:
1. Natrium mister en elektron: Natriumatomet opgiver sin enlige valenselektron og bliver til en positivt ladet natriumion (Na+).
2. Klor får en elektron: Kloratomet accepterer elektronen fra natrium og bliver til en negativt ladet chloridion (Cl-).
3. Ionbindingsdannelse: De modsat ladede ioner (Na+ og Cl-) tiltrækkes af hinanden af elektrostatiske kræfter og danner en ionbinding. Denne tiltrækning er stærk og resulterer i dannelsen af en krystalgitterstruktur i fast NaCl.
Resultat:
Udvekslingen af en elektron mellem natrium og klor skaber en stabil forbindelse, natriumchlorid (NaCl). Denne forbindelse er et hvidt, krystallinsk fast stof, der er almindeligt kendt som bordsalt.
Opsummering:
* Natriumatom mister en elektron for at blive en positivt ladet ion (Na+).
* Kloratom får en elektron til at blive en negativt ladet ion (Cl-).
* De modsat ladede ioner tiltrækker hinanden og danner en ionbinding og danner natriumchlorid (NaCl).
 Varme artikler
Varme artikler
-
 Cyanobakterier som grønne katalysatorer i bioteknologiCyanobakterier er miljøvenlige og let tilgængelige biokatalysatorer til produktion af nye kemikalier og, takket være forskere ved TU Graz, snart kunne bruges i store teknologiske applikationer. Kredit
Cyanobakterier som grønne katalysatorer i bioteknologiCyanobakterier er miljøvenlige og let tilgængelige biokatalysatorer til produktion af nye kemikalier og, takket være forskere ved TU Graz, snart kunne bruges i store teknologiske applikationer. Kredit -
 Forskere observerer katalysator under Fischer-Tropsch-syntese for første gangTestopsætning inklusive højtrykscelle til Fischer-Tropsch-målingskampagnen ved hjælp af CAT-ACT-målelinjen ved KIT-synkrotronen. Kredit:Tiziana Carambia Egnede katalysatorer er af stor betydning f
Forskere observerer katalysator under Fischer-Tropsch-syntese for første gangTestopsætning inklusive højtrykscelle til Fischer-Tropsch-målingskampagnen ved hjælp af CAT-ACT-målelinjen ved KIT-synkrotronen. Kredit:Tiziana Carambia Egnede katalysatorer er af stor betydning f -
 Hvordan man gør biokatalysatorer udødeligeNicolas Plumeré, Darren Buesen og Li Huaiguang (fra venstre). Kredit:RUB, Marquard Oxygen truer bæredygtige katalysatorer, der bruger hydrogen til at producere elektricitet i brændselsceller. Fors
Hvordan man gør biokatalysatorer udødeligeNicolas Plumeré, Darren Buesen og Li Huaiguang (fra venstre). Kredit:RUB, Marquard Oxygen truer bæredygtige katalysatorer, der bruger hydrogen til at producere elektricitet i brændselsceller. Fors -
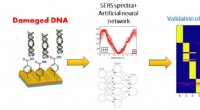 Forskere får neurale netværk til at opdage DNA-skader forårsaget af UV-strålingSkematisk diagram af SERS-sensorens drift i kombination med det neurale netværk til analyse af DNA-skader. Kredit:TPU Forskere ved Tomsk Polytekniske Universitet udførte sammen med Universitetet f
Forskere får neurale netværk til at opdage DNA-skader forårsaget af UV-strålingSkematisk diagram af SERS-sensorens drift i kombination med det neurale netværk til analyse af DNA-skader. Kredit:TPU Forskere ved Tomsk Polytekniske Universitet udførte sammen med Universitetet f
- Hvilken type energi giver damp?
- Hvilken del af en plantecelle kontrollerer de aktiviteter, som andre celler har?
- Hvordan er den anden lov om termodynamik relateret til økologi?
- Hvilket fast stof kan være i en væske?
- Hvad beskytter jorden mod skadelige solbrændere?
- Borophen på sølv vokser frit til en atomisk hud


