Polære forbindelser:Forståelse af elektronegativitet og molekylær polaritet
Her er en oversigt:
* Elektronegativitet: Dette er et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding. Forskellige grundstoffer har forskellige elektronegativiteter.
* Polær kovalent binding: Når to atomer med forskellige elektronegativiteter danner en binding, trækkes elektronerne mere mod atomet med højere elektronegativitet. Dette skaber en delvis negativ ladning (δ-) på det mere elektronegative atom og en delvis positiv ladning (δ+) på det mindre elektronegative atom.
* Polært molekyle: Hvis et molekyle har polære kovalente bindinger, og bindingerne er arrangeret asymmetrisk, vil molekylet have et netto dipolmoment, hvilket betyder, at det vil have en positiv og en negativ ende.
Karakteristika for polære forbindelser:
* Opløselighed i vand: Polære forbindelser har en tendens til at opløses i vand, fordi vand også er et polært molekyle. Den positive ende af vandmolekylet kan tiltrække den negative ende af den polære forbindelse og omvendt.
* Høje kogepunkter: Polære forbindelser har en tendens til at have højere kogepunkter end ikke-polære forbindelser, fordi de intermolekylære kræfter mellem polære molekyler er stærkere.
* Gode ledere af elektricitet: Når de er opløst i vand, kan polære forbindelser lede elektricitet, fordi de ladede ioner er frie til at bevæge sig.
Eksempler på polære forbindelser:
* Vand (H₂O): Oxygenatomet er mere elektronegativt end hydrogenatomerne, hvilket resulterer i et polært molekyle.
* Ethanol (C2H5OH): Oxygenatomet i hydroxylgruppen (OH) er mere elektronegativt end carbon- og hydrogenatomerne.
* Hydrogenchlorid (HCl): Klor er mere elektronegativt end brint, hvilket gør molekylet polært.
I modsætning hertil ikke-polære forbindelser har en jævn fordeling af elektroner og har ikke en positiv eller negativ ende. De har typisk lave kogepunkter og er ikke opløselige i vand. Eksempler omfatter methan (CH4) og olie.
 Varme artikler
Varme artikler
-
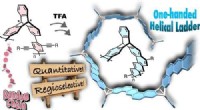 Syntese af spiralformede stigepolymererRapport:En effektiv syntese af optisk aktive stige-type molekyler og polymerer gennem intramolekylær ringslutning af chirale triptycener indeholdende bis[2-(4-alkoxyphenyl)ethynyl]phenylenenheder. De
Syntese af spiralformede stigepolymererRapport:En effektiv syntese af optisk aktive stige-type molekyler og polymerer gennem intramolekylær ringslutning af chirale triptycener indeholdende bis[2-(4-alkoxyphenyl)ethynyl]phenylenenheder. De -
 Video:Hvad skal der til for at forvandle Boston havn til te?Kredit:The American Chemical Society Den 16. december 1773, demonstranterne i Bostons tefest smed mere end 340 kister fulde af te – svarende til omkring 18 og en halv million teposer – ind i havne
Video:Hvad skal der til for at forvandle Boston havn til te?Kredit:The American Chemical Society Den 16. december 1773, demonstranterne i Bostons tefest smed mere end 340 kister fulde af te – svarende til omkring 18 og en halv million teposer – ind i havne -
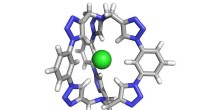 Opbygning af en bedre saltlås:Forskere syntetiserer et molekylærbur for at fange kloridEn computergengivelse af seks-triazolmolekyleburet designet til at fange kloridsalte. Kredit:Yan Liu, University of Illinois i Urbana-Champaign Indiana University forskere har skabt et kraftfuldt
Opbygning af en bedre saltlås:Forskere syntetiserer et molekylærbur for at fange kloridEn computergengivelse af seks-triazolmolekyleburet designet til at fange kloridsalte. Kredit:Yan Liu, University of Illinois i Urbana-Champaign Indiana University forskere har skabt et kraftfuldt -
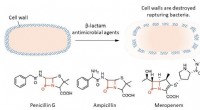 En ny synder i antibakteriel resistens:CysteinpersulfidØverst:β-lactam antimikrobielle midler sprænger bakterier ved at ødelægge deres cellevægge. Nederst:Den røde tekst i strukturformlen repræsenterer β-lactamringen, som er afgørende for bakteriedræbende
En ny synder i antibakteriel resistens:CysteinpersulfidØverst:β-lactam antimikrobielle midler sprænger bakterier ved at ødelægge deres cellevægge. Nederst:Den røde tekst i strukturformlen repræsenterer β-lactamringen, som er afgørende for bakteriedræbende
- Hvad er signalhypotese?
- Hvad er geotermisk?
- Hvordan sammenligner planter sig med solceller, når det kommer til opsamling af solenergi?
- Jordens stabile temperatur tidligere tyder på, at andre planeter også kan opretholde liv
- Hvad er forskellen mellem hydrogenchlorid og vandfrit chlorid?
- Hvordan påvirker geotermisk energi dine liv?


