Metallisk binding og høje smeltepunkter i metaller:en forklaring
* Metallisk binding: Ved metallisk binding delokaliseres metalatomernes valenselektroner og danner et "hav" af elektroner, der frit kan bevæge sig gennem hele metalstrukturen. Dette skaber en stærk, ikke-retningsbestemt tiltrækning mellem de positivt ladede metalioner og det negativt ladede elektronhav.
* Høje smeltepunkter: Den stærke elektrostatiske tiltrækning mellem ionerne og elektronhavet kræver en betydelig mængde energi at overvinde. Det betyder, at der skal meget varme til for at bryde de metalliske bindinger fra hinanden og overføre metallet fra et fast stof til en væske.
Andre typer binding:
* Ionisk binding: Mens ionbindinger er stærke, er de generelt svagere end metalliske bindinger.
* Kovalent binding: Kovalente bindinger er meget stærke i molekylet, men kræfterne mellem molekylerne er svagere.
* Van der Waals styrker: Det er meget svage kræfter, der bidrager til tiltrækningen mellem molekyler.
Sammenfattende gør den stærke og ikke-retningsbestemte karakter af metallisk binding metaller til høje smeltepunkter.
 Varme artikler
Varme artikler
-
 Fosforescerende materiale inspireret af glød i det mørke træBroderi med fluorescerende tråd på venstre blad, og fosforescerende tråd på de to blomster. Begge lyser under et UV-lys (midt), men kun den fosforescerende tråd lyser i mørke kortvarigt (højre). Kredi
Fosforescerende materiale inspireret af glød i det mørke træBroderi med fluorescerende tråd på venstre blad, og fosforescerende tråd på de to blomster. Begge lyser under et UV-lys (midt), men kun den fosforescerende tråd lyser i mørke kortvarigt (højre). Kredi -
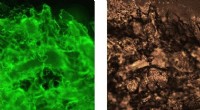 Forskere udvikler gel lavet af edderkoppesilkeproteiner til biomedicinske anvendelserHydrogelerne farves med et fluorescerende farvestof, der binder til amyloidstrukturer og det tilsvarende lysfeltbillede. Kredit:Tina Arndt Forskere ved KI og SLU har opdaget, at edderkoppesilkeprot
Forskere udvikler gel lavet af edderkoppesilkeproteiner til biomedicinske anvendelserHydrogelerne farves med et fluorescerende farvestof, der binder til amyloidstrukturer og det tilsvarende lysfeltbillede. Kredit:Tina Arndt Forskere ved KI og SLU har opdaget, at edderkoppesilkeprot -
 Et nyt materiale til fremtidens batteriUCLouvains forskere opdagede et nyt højtydende og sikkert batterimateriale (LTPS), der kan fremskynde opladning og afladning til et niveau, der aldrig er observeret hidtil. Kredit:University of Louvai
Et nyt materiale til fremtidens batteriUCLouvains forskere opdagede et nyt højtydende og sikkert batterimateriale (LTPS), der kan fremskynde opladning og afladning til et niveau, der aldrig er observeret hidtil. Kredit:University of Louvai -
 En opskalering af nanoporøs membrancentrifuge til afsaltning af omvendt osmose uden tilsmudsningFigur 1. Design og bevis på konceptet for nano-porøs membrancentrifuge:(a), (b), og (c) detaljer i nanoskala af vandmolekyler og Na+/Cl-ioner i nærheden af grafenmembranen; (d) illustration rotation
En opskalering af nanoporøs membrancentrifuge til afsaltning af omvendt osmose uden tilsmudsningFigur 1. Design og bevis på konceptet for nano-porøs membrancentrifuge:(a), (b), og (c) detaljer i nanoskala af vandmolekyler og Na+/Cl-ioner i nærheden af grafenmembranen; (d) illustration rotation


