Magnesium- og saltsyrereaktion:En detaljeret forklaring
Her er den afbalancerede kemiske ligning for reaktionen:
Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
Forklaring:
* Magnesium (Mg) er et reaktivt metal.
* Saltsyre (HCl) er en stærk syre, hvilket betyder, at den let donerer hydrogenioner (H+).
* Når magnesium kommer i kontakt med saltsyre, sker der følgende:
* Brintioner (H+) fra syren reagerer med magnesiumatomerne og fortrænger dem fra magnesiummetallet.
* Dette danner magnesiumchlorid (MgCl₂) et opløseligt salt.
* De fortrængte hydrogenioner kombineres og danner brintgas (H₂) , som frigives som bobler.
Observationer:
* Du vil observere kraftig bobling da der produceres brintgas.
* Løsningen vil varme op på grund af reaktionens eksoterme karakter.
* Magnesiummetallet vil opløses da det reagerer med syren.
Sikkerhedsforanstaltninger:
* Denne reaktion er exoterm og producerer brintgas, som er brandfarlig.
* Bær passende beskyttelsesbriller og handsker, når du udfører dette eksperiment.
* Udfør reaktionen i et godt ventileret område.
* Bland aldrig store mængder magnesium og saltsyre, da det kan føre til en voldsom reaktion.
 Varme artikler
Varme artikler
-
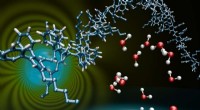 Et vindue til fældefri ladningstransport i organiske halvledereEn kunstners indtryk af en klynge af vandmolekyler, der fungerer som en hulfælde. Kredit:D. Andrienko, MPI-P. Organiske halvledere, en klasse af kulstofbaserede materialer med optiske og elektroni
Et vindue til fældefri ladningstransport i organiske halvledereEn kunstners indtryk af en klynge af vandmolekyler, der fungerer som en hulfælde. Kredit:D. Andrienko, MPI-P. Organiske halvledere, en klasse af kulstofbaserede materialer med optiske og elektroni -
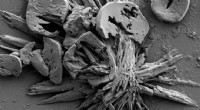 Portrætter af partiklerKredit:Duke University På solparker på særligt støvede steder i verden, ligesom den arabiske halvø og dele af Indien og Kina, luftforurening koster solenergiindustrien titusinder af milliarder af
Portrætter af partiklerKredit:Duke University På solparker på særligt støvede steder i verden, ligesom den arabiske halvø og dele af Indien og Kina, luftforurening koster solenergiindustrien titusinder af milliarder af -
 Ny hydrogel udnytter luftfugtighed til praktiske anvendelserNy vandabsorberende gel opfundet af NUS Engineering-forskere udnytter luftfugtighed til praktiske anvendelser. Kredit:National University of Singapore Høj luftfugtighed giver ubehag og får varme d
Ny hydrogel udnytter luftfugtighed til praktiske anvendelserNy vandabsorberende gel opfundet af NUS Engineering-forskere udnytter luftfugtighed til praktiske anvendelser. Kredit:National University of Singapore Høj luftfugtighed giver ubehag og får varme d -
 Video:Kan vi gøre opioider mindre vanedannende?Kredit:The American Chemical Society Opioider er de mest kraftfulde smertestillende midler, vi har, men de er utroligt vanedannende. Titusindvis af mennesker i USA dør af en opioidoverdosis hvert
Video:Kan vi gøre opioider mindre vanedannende?Kredit:The American Chemical Society Opioider er de mest kraftfulde smertestillende midler, vi har, men de er utroligt vanedannende. Titusindvis af mennesker i USA dør af en opioidoverdosis hvert
- Titanium trykbeholder til rumudforskning bygget med succes ved hjælp af Wire + Arc additiv fremstil…
- Hvad er Hox -gener?
- Hvad spiser skilpadder?
- Kloning resulterer i to organismer, der er?
- Ny katalysator gør ammoniak til et innovativt rent brændstof
- Forskere bruger årstider til at finde vand til fremtidige Mars-astronauter


