Forståelse af 1N svovlsyrerenhed:Hvad du behøver at vide
* Normalitet (N) repræsenterer antallet af ækvivalenter af et stof pr. liter opløsning. Det er en koncentrationsenhed, der er specielt designet til reaktioner, i betragtning af antallet af ioner, der kan deltage.
* Renhed i procent angiver andelen af et ønsket stof i en prøve, normalt udtrykt som en procentdel af den samlede masse.
For at beregne den procentvise renhed har du brug for yderligere oplysninger:
1. Densitet af 1N svovlsyreopløsningen: Dette fortæller dig massen af opløsningen pr. volumenhed.
2. Molar masse af svovlsyre (H₂SO₄): Dette er en konstant værdi (98,079 g/mol).
Sådan vil du gå videre:
1. Konverter normalitet til molaritet: 1N svovlsyre svarer til 0,5M svovlsyre (da svovlsyre har to sure protoner).
2. Beregn massen af svovlsyre pr. liter:
* Multiplicer molariteten med molmassen:0,5 mol/L * 98,079 g/mol =49,0395 g/L
3. Beregn opløsningens masse pr. liter:
* Multiplicer tætheden med 1000 (for at konvertere fra g/mL til g/L).
4. Beregn den procentvise renhed:
* Divider massen af svovlsyre pr. liter med massen af opløsningen pr. liter og gang med 100.
Eksempel:
Lad os antage, at densiteten af din 1N svovlsyreopløsning er 1,05 g/ml.
1. Masse af opløsning pr. liter:1,05 g/mL * 1000 mL/L =1050 g/L
2. Renhedsprocent:(49,0395 g/L / 1050 g/L) * 100 % =4,67 %
Vigtigt: Dette er blot et eksempel på en beregning. Du har brug for den faktiske massefylde af din specifikke 1N svovlsyreopløsning for at få den korrekte procentvise renhed.
 Varme artikler
Varme artikler
-
 Skaller og grapefrugter inspirerer til først fremstillet ikke-skærbart materialeKredit:CC0 Public Domain Ingeniører har hentet deres inspiration fra skaller og grapefrugter til at skabe, hvad de siger er det første fremstillede ikke-skærbare materiale. Dette nye materiale, s
Skaller og grapefrugter inspirerer til først fremstillet ikke-skærbart materialeKredit:CC0 Public Domain Ingeniører har hentet deres inspiration fra skaller og grapefrugter til at skabe, hvad de siger er det første fremstillede ikke-skærbare materiale. Dette nye materiale, s -
 Sådan læser du et vandbarometer:En praktisk guide til vejrudsigtAf Henrietta Padgett • Opdateret 24. marts 2022 Vandbarometre kombinerer elegant design med praktisk anvendelighed, så du kan måle atmosfærisk tryk og forudse vejrskift med minimal indsats. Selvom en
Sådan læser du et vandbarometer:En praktisk guide til vejrudsigtAf Henrietta Padgett • Opdateret 24. marts 2022 Vandbarometre kombinerer elegant design med praktisk anvendelighed, så du kan måle atmosfærisk tryk og forudse vejrskift med minimal indsats. Selvom en -
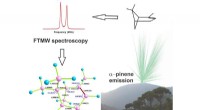 Molekylstrukturen i en skovaroma dekonstrueretGasfasestruktur af alfa-pinen er blevet eksperimentelt afsløret, ved hjælp af Fourier transform mikrobølgespektroskopi og kvantekemiske beregninger. Kredit:Elias M. Neeman Det friske, en umiskende
Molekylstrukturen i en skovaroma dekonstrueretGasfasestruktur af alfa-pinen er blevet eksperimentelt afsløret, ved hjælp af Fourier transform mikrobølgespektroskopi og kvantekemiske beregninger. Kredit:Elias M. Neeman Det friske, en umiskende -
 Valg af den rigtige flaske til opbevaring af syrer og baser:En praktisk vejledningAf Rochelle Leggett Opdateret 24. marts 2022 MadamLead/iStock/GettyImages Stærke syrer og baser udgør væsentlige sundhedsfarer, så valg af den korrekte beholder er afgørende for sikkerheden og over
Valg af den rigtige flaske til opbevaring af syrer og baser:En praktisk vejledningAf Rochelle Leggett Opdateret 24. marts 2022 MadamLead/iStock/GettyImages Stærke syrer og baser udgør væsentlige sundhedsfarer, så valg af den korrekte beholder er afgørende for sikkerheden og over
- Hvilke energioverførsler eller ændringer sker, når du bruger en nedsænkningsvarmer til varmt van…
- Optimalitet i selvorganiseret molekylær sortering
- Hvornår blev Apollo bygget?
- Hvad er forholdet mellem kraft og lineær momentum?
- Af hvilket stof er de ydre planeter for det meste sammensat?
- 100 millimeter hvor mange centimeter?


