Letteste oxiderede metaller:Placering i det periodiske system forklaret
* Elektropositivitet: Metaller i denne region har en høj tendens til at miste elektroner og blive positivt ladede ioner (kationer). Dette skyldes deres lave ioniseringsenergier og store atomare radier.
* Metallig karakter: Metaller i denne region udviser stærk metallisk karakter. Det betyder, at de har løst fastholdte elektroner, der er let tilgængelige for oxidation.
Konkret er de lettest oxiderede metaller:
* Alkalimetaller (gruppe 1): Lithium (Li), natrium (Na), kalium (K), rubidium (Rb), cæsium (Cs) og francium (Fr).
* Alkaliske jordmetaller (gruppe 2): Beryllium (Be), magnesium (Mg), calcium (Ca), strontium (Sr), barium (Ba) og radium (Ra).
Undtagelser:
* Overgangsmetaller: Mens nogle overgangsmetaller er meget reaktive, er andre mere modstandsdygtige over for oxidation på grund af deres varierende elektronkonfigurationer og d-orbitale interaktioner.
Vigtig bemærkning: Oxidationspotentialet påvirkes af faktorer som:
* pH: Miljøets surhedsgrad eller basicitet kan påvirke oxidationshastigheden betydeligt.
* Temperatur: Højere temperaturer favoriserer generelt oxidationsreaktioner.
* Tilstedeværelse af oxidationsmidler: Tilstedeværelsen af oxidationsmidler som oxygen eller halogener kan fremskynde oxidationsprocessen.
 Varme artikler
Varme artikler
-
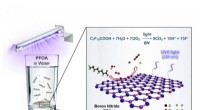 Bornitrid ødelægger for evigt kemikalier PFOA, GenXEn illustration af bornitrid-fotokatalyse, der ødelægger det forurenende stof PFOA i vand. Kredit:Billede udlånt af M. Wong/Rice University Rice University kemiingeniører fandt en effektiv katalys
Bornitrid ødelægger for evigt kemikalier PFOA, GenXEn illustration af bornitrid-fotokatalyse, der ødelægger det forurenende stof PFOA i vand. Kredit:Billede udlånt af M. Wong/Rice University Rice University kemiingeniører fandt en effektiv katalys -
 Nye fotoniske flydende krystaller kan føre til næste generations skærmeEt nærbillede af en blåfaset flydende krystal i mm-størrelse under dannelsesstadiet. Kredit:Khoo Lab, Penn State En ny teknik til at ændre strukturen af flydende krystaller kan føre til udviklin
Nye fotoniske flydende krystaller kan føre til næste generations skærmeEt nærbillede af en blåfaset flydende krystal i mm-størrelse under dannelsesstadiet. Kredit:Khoo Lab, Penn State En ny teknik til at ændre strukturen af flydende krystaller kan føre til udviklin -
 Hvilke planter kan lære os om rensning af olieudslip og mikrofluidikÅrevis, forskere er blevet inspireret af naturen til at innovere løsninger på vanskelige problemer, selv olieudslip - menneskeskabte katastrofer med ødelæggende miljømæssige og økonomiske konsekvenser
Hvilke planter kan lære os om rensning af olieudslip og mikrofluidikÅrevis, forskere er blevet inspireret af naturen til at innovere løsninger på vanskelige problemer, selv olieudslip - menneskeskabte katastrofer med ødelæggende miljømæssige og økonomiske konsekvenser -
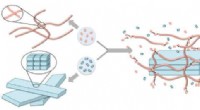 Molekylært stillads hjælper konstruktion på nanoskalaKredit:Okinawa Institute of Science and Technology Graduate University Hvis du vil bygge et højt hus, du skal bruge stillads. Professor Ye Zhang og kolleger ved Okinawa Institute of Science and Te
Molekylært stillads hjælper konstruktion på nanoskalaKredit:Okinawa Institute of Science and Technology Graduate University Hvis du vil bygge et højt hus, du skal bruge stillads. Professor Ye Zhang og kolleger ved Okinawa Institute of Science and Te
- Hvordan er erosion og afbildning relateret?
- Stedet for det næste store jordskælv på San Andreas Fault?
- Nogle smarte måder at søge efter primordiale sorte huller på
- Hvad er den kronologiske samling af rester, der findes i lags rock?
- Hvilke elementer udgør troposfæren?
- Epigenetisk indsigt:Hvordan hybridpoppel regenererer skud


